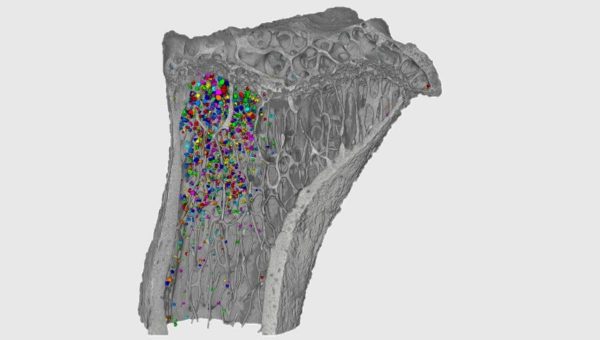
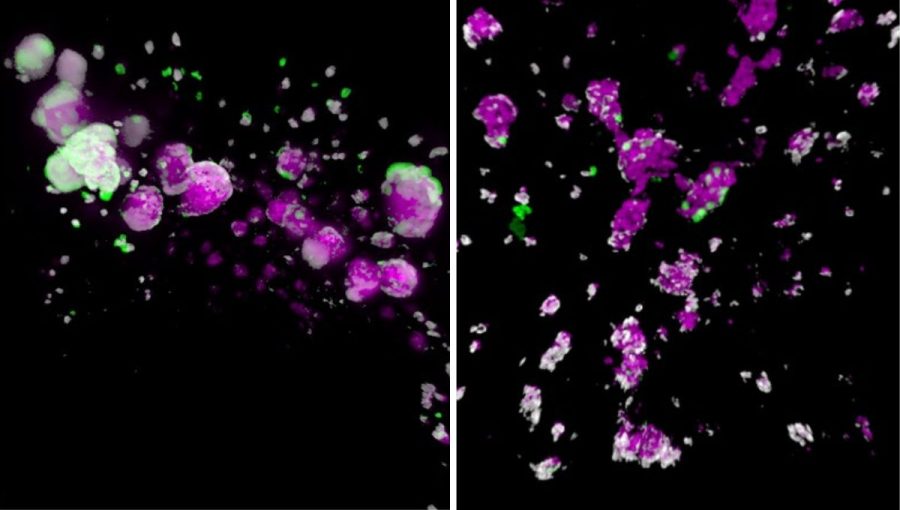
Editované darcovské bunky produkujú inzulín a dokážu obísť imunitnú reakciu organizmu, príjemca tak nemusí užívať imunosupresívne lieky.

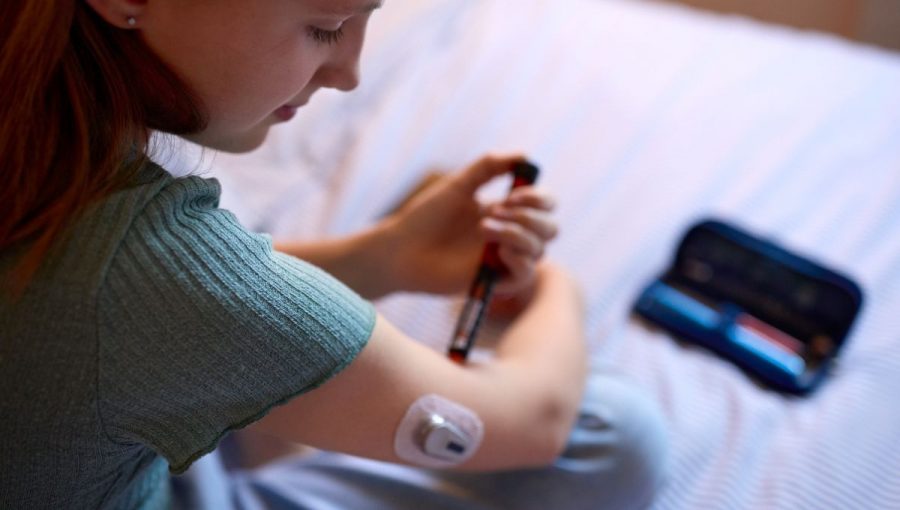
Nová metóda by mohla priniesť to, v čo ľudia s cukrovkou 1. typu dúfajú už dlho. Veria v jednorazovú liečbu, dostupnú pre každého, kto ju potrebuje, ktorá obnoví produkciu inzulínu bez ihiel, púmp a liekov potláčajúcich imunitu. Ilustračný obrázok. Zdroj: iStock.com/Iconic Prototype
Vedci po prvýkrát implantovali pacientovi s diabetom 1. typu pankreatické bunky od zosnulého darcu editované metódou CRISPR. Bunky produkovali inzulín niekoľko mesiacov. Príjemca nemusel užívať lieky potláčajúce imunitnú reakciu, pretože jeho imunitný systém špeciálne upravené bunky ani nezaznamenal.
Štúdia, ktorú uskutočnila biotechnologická spoločnosť Sana, vzbudzuje nádej na vyliečenie cukrovky 1. typu, autoimunitného ochorenia, v dôsledku ktorého sú milióny ľudí odkázané na celoživotnú inzulínovú substitúciu. O novom prístupe informuje časopis Nature.
Imunitné maskovanie
Hlavným cieľom je aplikovať opravené gény zabezpečujúce imunitné maskovanie na kmeňové bunky a potom ich vývoj nasmerovať do buniek ostrovčekov produkujúcich inzulín. Podľa výsledkov malej štúdie, ktoré boli uverejnené v júni, sú needitované ostrovčeky vytvorené z kmeňových buniek sľubným prístupom v liečbe cukrovky 1. typu.
Niektoré nezávislé výskumné skupiny však nedokázali potvrdiť, že metóda spoločnosti Sana umožňuje editovaným bunkám obchádzať imunitný systém. Do štúdie bol zapojený len jeden človek, ktorému bola podaná nízka dávka buniek na krátky čas. Ako uviedol Tim Kieffer, molekulárny endokrinológ z Univerzity Britskej Kolumbie vo Vancouveri v Kanade, nestačilo to „na dosiahnutie nezávislosti od inzulínu, takže klinická účinnosť zostáva nepotvrdená“.
Aj napriek tomu Kieffer považuje demonštráciu imunitného maskovania za „presvedčivú“ a za „významný míľnik na ceste k dosiahnutiu efektívnej bunkovej terapie bez chronickej imunosupresie“. Kieffer predtým zastával funkciu vedúceho vedeckého pracovníka v biotechnologickej spoločnosti ViaCyte (neskôr ju prevzala spoločnosť Vertex Pharmaceuticals v Bostone, Massachusetts), ktorá sa podobne ako Sana zameriavala na vývoj bunkových terapií pre cukrovku 1. typu.
Liečba kmeňovými bunkami
Jediný spôsob, ako môžu pacienti s cukrovkou 1. typu v súčasnosti fungovať bez inzulínu, sú transplantované bunky ostrovčekov od darcu. Vďaka tomuto zákroku dokáže telo produkovať inzulín niekoľko rokov. Podobné zákroky sú však veľmi zriedkavé. Jednou z príčin je nedostatok darcovských pankreasov. Ďalším dôvodom je následná nutnosť celoživotnej liečby imunosupresívami, čo so sebou nesie riziko infekcie, rakoviny a ďalších závažných vedľajších účinkov.
Nedostatok darcov riešia niektoré spoločnosti využívaním technológií na báze kmeňových buniek, ktoré umožňujú vytvárať náhradné ostrovčeky laboratórnou cestou.
V tomto ohľade pokročila najďalej spoločnosť Vertex. Tá v júni oznámila, že transplantovala ostrovčeky vypestované z embryonálnych kmeňových buniek 12 ľuďom s cukrovkou 1. typu. Po jednom roku už desať účastníkov nepotrebovalo inzulínovú liečbu. Spoločnosť plánuje v budúcom roku požiadať o regulačné schválenie tejto bunkovej terapie.
Na podobnom princípe pracuje spoločnosť Reprogenix Bioscience z čínskeho Hangzhou, ktorá sa špecializuje na regeneratívnu medicínu. Ostrovčeky z preprogramovaných kmeňových buniek získava z tukového tkaniva príjemcu. Reprogenix Bioscience už vydala prvé vyhlásenia o úspešnosti postupu. Oba prístupy však stále vyžadujú, aby príjemcovia užívali lieky potláčajúce imunitnú odpoveď organizmu, a to buď na odrazenie imunitných útokov na darcovské bunky, alebo na potlačenie autoimunitnej reakcie príjemcu.
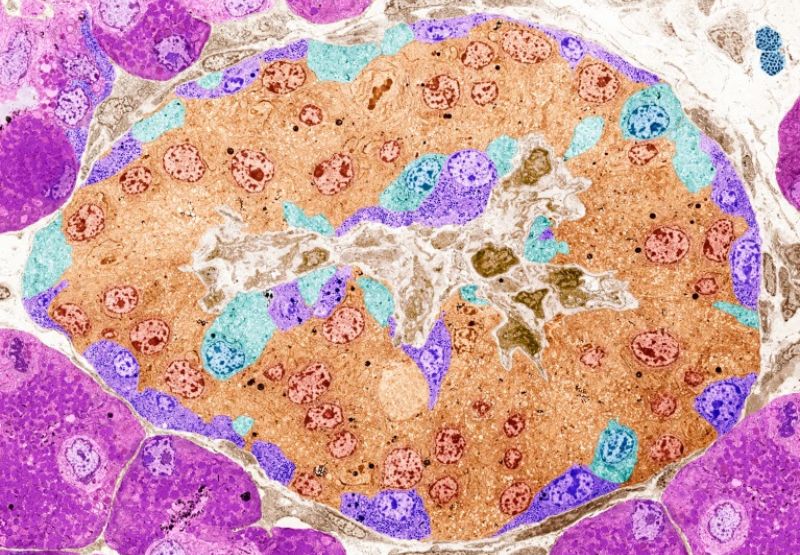
Pankreatické ostrovčeky (umelo sfarbené) u ľudí s cukrovkou 1. typu nevylučujú dostatočné množstvo inzulínu. Zdroj: Nature. Credit: Steve Gschmeissner/SPL
V utajení
Spoločnosť Sana sa snaží potrebu imunosupresívnej liečby obísť. Vedci použili v prípade prvého príjemcu bunky od zdravého darcu, ktoré implantovali príjemcovi. Opravou génov metódou CRISPR výskumníci deaktivovali dva gény, ktoré T-bunkám, prvej obrannej línii organizmu, pomáhajú identifikovať cudzie invázne bunky.
Následne použili vírus na prenos genetických inštrukcií pre proteín nazývaný CD47 do buniek. Tento proteín signalizuje niečo v zmysle nezjedz ma, a tak zabraňuje strážcom imunity, známym ako prirodzené zabíjačské bunky, aby napádali editované bunky.
Klinickí lekári vo Švédsku aplikovali mužovi s ťažkou cukrovkou injekčne bezpečnú dávku obsahujúcu približne 80 miliónov takto modifikovaných buniek. Imunitný systém muža rýchlo eliminoval všetky bunky, ktorým chýbala jedna génová úprava alebo im chýbali viaceré. Bunky s kompletným súborom ochranných zmien však „prežili“ a produkovali inzulín bez imunitného zásahu počas 12 týždňov. Najnovšie uverejnené správy dokonca uvádzajú až 6 mesiacov.
Sonja Schrepferová, vedkyňa, zakladateľka spoločnosti Sana a transplantačná imunologička, ktorá v súčasnosti pôsobí v Cedars–Sinai Medical Center v Los Angeles v Kalifornii a je aj spoluautorkou štúdie, uviedla, že geneticky editované bunky „skutočne prekonávajú transplantačnú bariéru“.
Pojem transplantačná bariéra (transplant barrier) sa používa na označenie prekážok, ktoré stoja v ceste jednoduchému prenosu bunky, tkaniva alebo orgánu od darcu k príjemcovi. Najväčšia bariéra je imunitný systém, ktorý cudzie bunky rozpozná a zničí.
Kevan Herold, imunológ na Yale School of Medicine v New Havene v Connecticute, spoluautor článku, uverejneného v septembrovom vydaní časopisu New England Journal of Medicine, považuje všetky tieto klinické pokroky za prvé míľniky v liečbe, ktorá by mohla priniesť to, v čo ľudia s cukrovkou 1. typu dúfajú už dlho. Dúfajú v jednorazovú liečbu, dostupnú pre každého, kto ju potrebuje, ktorá obnoví produkciu inzulínu bez ihiel, púmp a liekov potláčajúcich imunitu.
Skutočný úspech však podľa neho prinesie kombinácia stratégií, napríklad spojenie úprav maskujúcich imunitu s ostrovčekmi odvodenými z kmeňových buniek.
Hľadanie skrytých liekov
Touto cestou sa v súčasnosti uberá výskum spoločností ako Vertex či Sana. Podľa Steva Harra, spoluzakladateľa a výkonného riaditeľa spoločnosti Sana, sú klinické štúdie naplánované už na budúci rok.
Potvrdený úspech v takejto štúdii by mohol pomôcť utíšiť kritiku imunitného maskovacieho prístupu spoločnosti Sana, ktorý sa opiera o CD47, aby udržal prirodzené zabíjačské bunky na uzde. Niekoľko nezávislých skupín sa totiž pokúšalo neúspešne replikovať ochranné účinky CD47 v laboratóriu. „Bolo nás veľa, ktorí sme sa o to pokúsili, a neuspeli sme,“ uviedol Deepta Bhattacharya, imunológ z Arizonskej univerzity v Tucsone.
Zároveň však dodal: „Ak začnú skutočne liečiť ľudí s cukrovkou 1. typu, potom budem mlčať a poviem: ‚mea culpa‘.“
Zdroj: Nature
(zh)