Bábätko s vážnym genetickým ochorením podstúpilo prvú personalizovanú CRISPR terapiu na svete. Podľa vedcov ide o míľnik v medicíne.
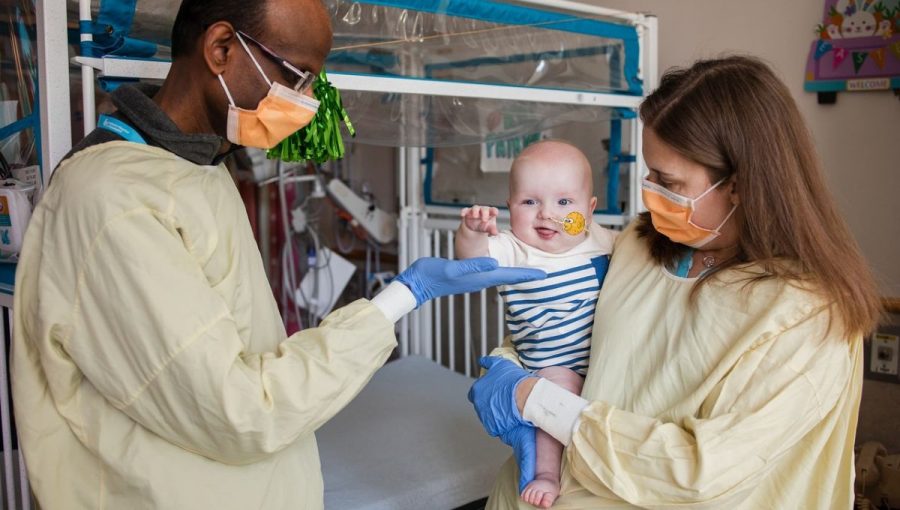
Špecialisti Rebecca Ahrensová-Nicklasová a Kiran Musunuru s malým pacientom menom KJ. Zdroj: www.chop.edu
Prvá CRISPR génová terapia vyvinutá len pre konkrétneho pacienta bola po prvýkrát použitá u detského pacienta. Bol ním len desaťmesačný chlapec v USA, ktorý trpí vážnym dedičným ochorením.
Odborníci použili technológiu Crispr-Cas9 – známu aj ako génové nožnice –, za ktorú získali v roku 2020 Nobelovu cenu dve vedkyne, a to francúzska biochemička Emmanuelle Charpentierová a jej americká kolegyňa Jennifer Doudnová.
Tím vedcov, ktorý liečbu vyvinul a dozeral na ňu, ju považuje za míľnik v oblasti personalizovanej genetickej medicíny. Terapia predstavuje nádej pre ďalších pacientov trpiacich vážnymi genetickými ochoreniami.
Zriedkavé genetické ochorenie
Príbeh malého chlapca menom KJ Muldoon, o ktorom na svojich stránkach informuje Detská nemocnica vo Filadelfii, predznamenáva budúcnosť personalizovanej medicíny.
Takmer desaťmesačnému chlapcovi bolo krátko po narodení diagnostikované dedičné metabolické ochorenie patriace medzi poruchy cyklu močoviny. Ide o zriedkavú diagnózu, ktorá postihuje jedného človeka z 1,3 milióna ľudí. Ochorenie spôsobujú zmeny v jednom z mnohých génov zodpovedných za cyklus močoviny. Ide o gény zodpovedajúce za výrobu enzýmov, ktoré v pečeni premieňajú amoniak, vznikajúci rozkladom bielkovín v tele, na močovinu. Ak sa v tele nevytvára dostatočné množstvo jedného alebo viacerých z týchto enzýmov, hromadí sa v ňom amoniak, ktorý je toxický pre mozog a pečeň.
Personalizovaná liečba šitá na mieru
Génovej terapii zameranej na liečbu tohto zriedkavého ochorenia sa už dva roky venoval tím odborníkov z Detskej nemocnice vo Filadelfii (Children’s Hospital of Philadelphia – CHOP) a Pensylvánskej univerzity. KJ mal teda šťastie, lebo bol zaradený do vedeckého programu a vedci mu personalizovanú génovú terapiu ušili doslova na mieru.
Komplexný návrh, vývoj a testovanie personalizovanej liečby dokončili vedci do šiestich mesiacov od stanovenia diagnózy. Následne dostal KJ prostredníctvom infúzie tri dávky personalizovaného lieku. Prvá mu bola podaná vo februári a ďalšie dve dávky v marci a apríli. KJ sa stal vôbec prvým pacientom, ktorý dostal systémový personalizovaný liek na úpravu génov. Chlapec bol medzitým napojený na dialýzu, ktorou sa filtroval amoniak z jeho tela a tým sa stabilizoval jeho stav.
Dr. Rebecca Ahrensová-Nicklasová, vedúca lekárka tímu odborníkov a pediatrička z Detskej nemocnice vo Filadelfii v Pensylvánii, uviedla, že ide o pokrok v liečbe a „hoci je KJ len jedným pacientom, dúfame, že je prvým z mnohých, ktorí z neho budú mať úžitok“.
Deficit CPS1
V článku v časopise The New England Journal of Medicine lekári opísali náročný proces identifikácie špecifických mutácií, ktoré stoja za chlapcovou poruchou, návrh terapie génovou úpravou na ich korekciu a testovanie liečby a nanočastíc potrebných na prenos do pečene.
Keď sa lekárom podarilo stabilizovať jeho stav, urobili genetické testy s cieľom zistiť presný typ poruchy cyklu močoviny, ktorým KJ trpí. Stanovenie postihnutého génu alebo enzýmu totiž malo vplyv na ďalší liečebný postup. Zistili, že ide o deficit karbamoylfosfátsyntetázy (CPS1), teda o vzácnu poruchu cyklu močoviny, ktorú spôsobuje gén CPS1.
Návrh liečby
V čase, keď lekári zvažovali ďalší postup chlapcovej liečby, bola jedinou život zachraňujúcou liečbou nedostatku CPS1 transplantácia pečene vhodnejšia skôr pre staršie deti.
Napriek tomu bol KJ zaradený do národného zoznamu čakateľov na transplantáciu s nádejou, že bude dostatočne stabilizovaný na transplantáciu pečene.
U detí s ťažkým ochorením však môže dôjsť počas hľadania vhodného darcovského orgánu k závažným poškodeniam organizmu, ktoré sú často fatálne. Aj preto sa chlapcovi rodičia rozhodli podstúpiť doteraz netestovanú liečbu.
Prelom v medicíne: personalizovaná úprava génov na záchranu chlapca menom KJ. Zdroj: Youtube/The Children’s Hospital of Philadelphia
Editácia báz
Terapia, ktorú vyvinul tím odborníkov, využíva účinný postup nazývaný editácia báz, ktorý dokáže prepísať kód DNA po jednom písmene.
Liek sa podával infúziou (v infúznej linke) a prúdil do krvného obehu, odkiaľ bol transportovaný do pečene. KJ dostal najnižšiu možnú dávku, aby mal jeho organizmus čas na adaptáciu a aby sa minimalizovali akékoľvek riziká.
„CRISPR, génový editor, vstupuje do jadra bunky,“ cituje tlačová správa nemocnice doktora Kirana Musunura. „V tomto prípade sme ho naprogramovali tak, aby sa dostal na miesto genetického variantu, ktorý chlapcovi spôsoboval ochorenie.“
Dr. Ahrensová-Nicklasová dodala: „Liek bol špeciálne navrhnutý pre pacienta a jeho genetické varianty. Ide o personalizovanú medicínu.“
Prognóza do budúcnosti
Podľa lekárov je malý pacient v dobrom stave, doživotne ho však budú lekári pozorovať. Po tom, ako bol KJ prvých pár mesiacov života v nemocnici na špeciálnej diéte, mohli už lekári zvýšiť množstvo bielkovín v jeho strave. Taktiež sa už podarilo znížiť dávky liekov na odstraňovanie amoniaku z tela. Lekársky tím uviedol, že na zistenie toho, do akej miery je terapia úspešná, budú potrebné ďalšie sledovania, prvé výsledky sú však povzbudivé.
Lekárka Rebecca Ahrensová-Nicklasová dúfa, že jedného dňa bude musieť KJ užívať len niekoľko liekov, možno dokonca žiadne lieky. „Dúfame, že bude prvým z mnohých, ktorí budú mať prospech z metódy, ktorú možno prispôsobiť individuálnym potrebám pacienta,“ uviedla lekárka.
Zdroj: The Children’s Hospital of Philadelphia, Nature, science.ORF.at, ČT24, analýza-DNA.cz
(zh)