Potenciálny liek na potlačenie hlavného rizikového faktora vzniku Alzheimerovej choroby je v pokročilej fáze klinického testovania.
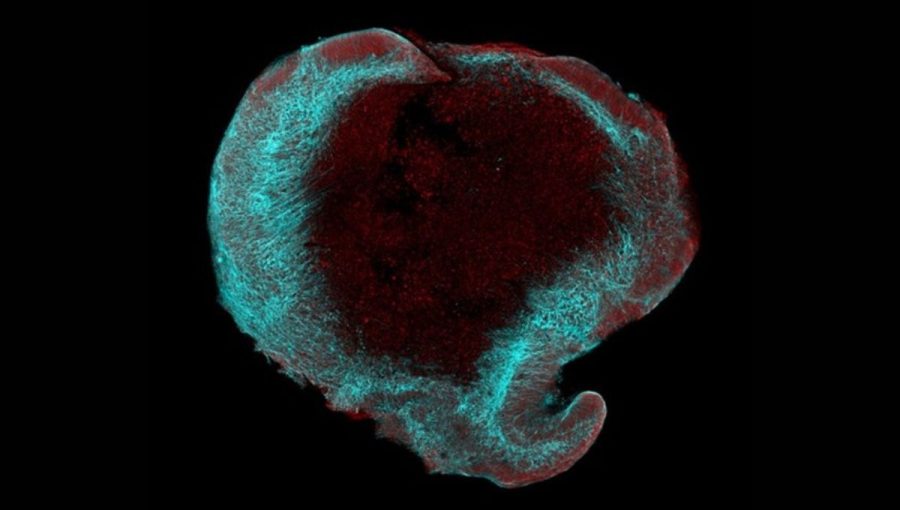
Mikroskopický záber mozgového organoidu. Experimenty s laboratórne kultivovanými mozgovými organoidmi preukázali pozitívny efekt homotaurínu. Zdroj: MUNI
Tím 23 brnianskych vedcov sa významne priblížil k zodpovedaniu otázky, ako predchádzať a liečiť Alzheimerovu chorobu, ktorá býva najčastejšou príčinou demencie a postupne vedie k odkázanosti pacienta na pomoc druhých pri vykonávaní bežných činností.
Odborníci z Prírodovedeckej a Lekárskej fakulty Masarykovej univerzity, Medzinárodného centra klinického výskumu a Masarykovho onkologického ústavu veria, že výsledky výskumu pomôžu vyvinúť ďalšie vysokoúčinné liečivé látky pre túto civilizačnú hrozbu 21. storočia.
O krok bližšie k liečbe
„Kľúčovú úlohu v rozvoji Alzheimerovej demencie má apolipoproteín E (ApoE), ktorý sa vyskytuje aj v mozgovom tkanive. Objavili sme molekulárnu podstatu nežiaduceho hromadenia sa tohto apolipoproteínu a súčasne sme ukázali spôsob, ako je možné toto hromadenie ApoE potlačiť potenciálnym liečivom, ktoré je už v pokročilej fáze klinického testovania s predpokladaným schválením v roku 2025,“ zhrnul hlavný význam výskumu molekulárny biológ Martin Marek, ktorý pôsobí v Loschmidtových laboratóriách centra RECETOX Prírodovedeckej fakulty Masarykovej univerzity a v Medzinárodnom centre klinického výskumu (ICRC), ktoré je spoločným pracoviskom Fakultnej nemocnice u sv. Anny v Brne a Lekárskej fakulty Masarykovej univerzity.
Práve ApoE zohráva dôležitú úlohu pri fungovaní mozgu. Známy je jeho protizápalový účinok. V ľudskej populácii sú rozšírené tri varianty: ApoE2, ApoE3 a ApoE4. Už skôr bolo dokázané, že hlavným rizikovým faktorom vzniku Alzheimerovej choroby je prítomnosť variantu ApoE4. Zdedenie variantu ApoE4 významne zvyšuje riziko demencie. U pacientov s dvoma kópiami génu pre ApoE4 dochádza k väčšiemu poškodeniu pamäti, k zníženej schopnosti vykonávať každodenné činnosti a k výraznejšej atrofii mozgového tkaniva. Už niekoľko desaťročí sa vedci z celého sveta pokúšajú objasniť tajomstvo ApoE4, no až brnianskym vedcom sa teraz podarilo nahliadnuť pod pokrievku tejto molekulárnej záhady.
„Vzrušujúce na tomto výskume bolo, že toxický variant ApoE4 sa líši od svojich netoxických náprotivkov len jednou mutáciou, ktorá však má obrovské dôsledky v správaní sa proteínu a vo vzťahu k rozvoju Alzheimerovej demencie,“ vysvetlil Marek.
Pozitívny efekt homotaurínu
Významnou súčasťou štúdie bol výskum, ako predchádzať nežiaducemu ukladaniu ApoE4 v mozgovom tkanive a obnoviť tak jeho dôležité bunkové funkcie. Laicky povedané, ako zabrániť rozvoju ochorenia, alebo ho spomaliť, a uchovať myslenie a pamäť. V nadväzných biochemických experimentoch výskumníci preukázali, že existuje látka homotaurín, derivát aminokyselín, nachádzajúci sa v niektorých druhoch morských rias. Táto látka potláča nežiaduce hromadenie a obnovuje pôvodné funkcie v ApoE4 proteíne. Mohla by tak mať liečebný efekt aj v klinickej praxi.
Pri experimentoch vedci používali mozgové organoidy, čo sú takzvané minimozočky vypestované v skúmavke z buniek pacientov s Alzheimerovou chorobou. „Mozgové organoidy sme v tejto štúdii použili na testovanie účinku homotaurínu na rozvoj Alzheimerovej demencie. Naše výsledky potvrdzujú, že liečivo má pozitívny efekt na organoidy s variantom ApoE4, a ukazuje sa, že ovplyvňuje nielen dôležité signalizačné dráhy, ale aj metabolizmus cholesterolu. V ďalších štúdiách sa chceme zamerať na podrobné mapovanie zmien, ktoré homotaurín v ľudskom mozgu spôsobuje,“ naznačila budúci terapeutický efekt homotaurínu a ďalší smer výskumu bunková biologička Dáša Bohačiaková z Ústavu histológie a embryológie Lekárskej fakulty Masarykovej univerzity.
Stabilizovanie apolipoproteínu ApoE4
Brnianskym vedcom sa podarilo kombináciou experimentálnych a výpočtových pokusov detailne zmapovať štruktúrne zmeny v ApoE proteíne na atómovej úrovni. Pôsobením týchto zmien variant proteínu ApoE4 nie je stabilný a má vysokú tendenciu k nežiaducemu hromadeniu v mozgovom tkanive, čím stráca svoju primárnu úlohu v prenose lipidov a cholesterolu.
„Dynamické zmeny v štruktúrach ApoE3 a ApoE4 proteínov a ich interakcie s potenciálnym liečivom (homotaurínom) sme sledovali pomocou unikátnej metódy výmeny vodíka za deutérium spojené s hmotnostnou spektrometriou. Výsledky odhalili prestavbu štruktúry v ApoE4, spôsobujúcu agregáciu, ktorá však nebola pozorovaná pri ApoE3. Naopak, interakcia s liečivom štruktúru ApoE4 stabilizovala, a tým potlačila jej negatívne vlastnosti,“ doplnila biochemička Lenka Hernychová z centra RECAMO Masarykovho onkologického ústavu.
Brnianski vedci publikovali výsledky výskumu v prestížnom odbornom časopise Molecular Neurodegeneration. Výskum získal podporu ministerstva školstva v rámci projektov ENOCH a INBIO. Výskum finančne podporila aj Európska únia v rámci programu Horizont Európa grantmi TEAMING a ADDIT-CE.
„Štúdia bola unikátna, pretože sa klasické metódy molekulárnej a bunkovej biológie podarilo doplniť o dáta získané technikou hmotnostnej spektrometrie. Takto možno veľmi citlivo a presne sledovať zmeny v hladinách proteínov a lipidov a nahliadnuť do mechanizmu účinku potenciálnych liečiv. Zároveň možno pomocou hmotnostnej spektrometrie charakterizovať často heterogénne bunkové modelové systémy,“ opísal jedinečnosť tohto výskumu analytický chemik Zdeněk Spáčil z centra RECETOX Prírodovedeckej fakulty Masarykovej univerzity.
Zdroj: TS MUNI
(zh)