Odpovede na otázky o biologických liekoch prináša brožúrka Štátneho ústavu pre kontrolu liečiv, ktorá vyšla s podporou Holandskej liekovej agentúry a brožúrka Európskej komisie: Čo potrebujem vedieť o biologicky podobných liekoch. V brožúrkach sa dozviete praktické informácie formou otázok a odpovedí o biologickej liečbe. V krátkosti vyberáme niektoré z nich, ktoré vysvetľujú základné pojmy v tejto inovatívnej liečbe.

Obálka brožúrky: Odpovede na otázky o biologických liekoch
Biologické lieky sa používajú na liečbu pacientov s dlhodobými ochoreniami či na liečbu vážnych ochorení, ktoré boli doteraz neliečiteľné. Používajú sa tiež na očkovanie (vakcináciu). Vývoj sa nezastavuje, objavujú sa nové biologické lieky aj na liečbu iných ochorení. Tieto lieky sa často podávajú injekčne alebo prostredníctvom infúzie.
Čo je to biologický liek?
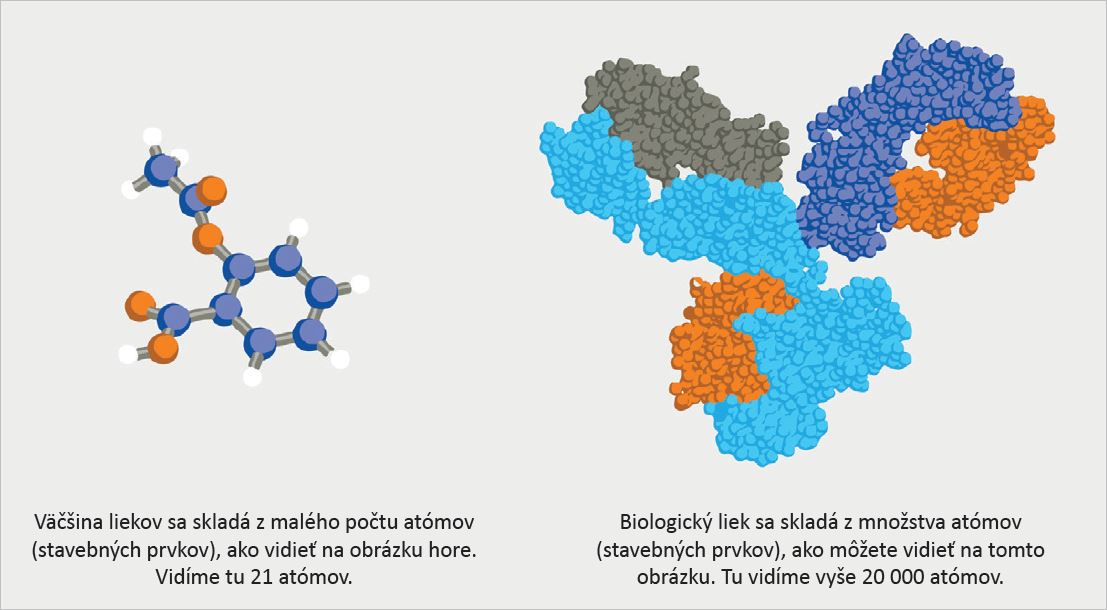
Ľudia si zvyčajne myslia, že lieky sú vyrobené z chemických látok. Biologické lieky (vrátane biologicky podobných liekov) však pochádzajú zo živých organizmov, ako sú živé bunky, ktoré boli upravené pomocou biotechnológie. To umožňuje týmto živým organizmom alebo bunkám vytvoriť účinnú látku biologického lieku. Následne sa táto účinná látka z buniek získa. Tieto účinné látky (napr. proteíny) sú zvyčajne väčšie a zložitejšie než účinné látky nebiologických liekov.
Biologické lieky sa od 80-tych rokov vyvíjajú pre rôzne ochorenia. K dostupným biologickým liekom patria aj hormóny ako inzulín a rastový hormón a aj monoklonálne protilátky na liečbu autoimunitných a nádorových ochorení. Niektoré z týchto účinných látok sa v tele prirodzene vyskytujú, napríklad účinné látky vyrobené z plazmy (zložka krvi), rastové hormóny alebo inzulín. Biologická liečba je jednou z najväčších inovácií v súčasnej medicíne.
Medzi biologickými liekmi môžu v každej šarži (výrobnej sérii) nastať drobné odchýlky. Stane sa tak preto, že liek vyrába živý organizmus a výroba takéhoto lieku pozostáva z množstva rozličných krokov. Štruktúra biologických liekov je tiež oproti bežným (chemickým) liekom mnohonásobne zložitejšia. Výrobca robí všetko preto, aby boli rozdiely čo najmenšie. Dosiahne to dodržiavaním schváleného výrobného postupu a dôkladnou kontrolou každého kroku v procese výroby lieku. Účinnosť lieku ostáva nezmenená.
Kedy vám môžu predpísať biologické lieky?
Lekár vám ich predpíše na liečbu rôznych ochorení, napr.:
• nedostatku hormónov (napr. inzulín pri cukrovke),
• autoimunitných chorôb, pri ktorých telo rozpoznáva vlastné bunky a/alebo látky ako cudzie, napr. pri reumatoidnej artritíde alebo Crohnovej chorobe,
• rakoviny,
• dedičných porúch krvnej zrážanlivosti (hemofílie),
• sklerózy multiplex,
• niektorých ochorení látkovej výmeny ako Pompeho či Fabryho choroba.
Čo je to biosimilárny liek?
Biosimilárny liek (t. j. biologicky podobný liek, niekedy nazývaný aj biosimilár), je biologický liek, ktorý sa veľmi podobá na originálny liek. Similar v angličtine znamená podobný. Keď je pôvodný biologický liek na trhu už niekoľko rokov, iní výrobcovia ho môžu „odkopírovať“. Keďže sa biologické lieky vyrábajú zo živých organizmov, nikdy nie sú úplne rovnaké. Rozdiely medzi biosimilárnym a originálnym liekom sú veľmi malé a vyskytujú sa aj pri jednotlivých šaržiach originálneho biologického lieku. Účinnosť a bezpečnosť biosimilárnych liekov sa však vždy zhoduje s originálnym biologickým liekom, tiež nazývaným referenčným liekom. Biosimilárny liek teda funguje rovnako dobre ako referenčný liek.
Biologické aj biosimilárne lieky sa registrujú v Európskej liekovej agentúre. Prvý biosimilárny liek bol registrovaný v roku 2006. Všetky lieky sú starostlivo monitorované a doteraz neboli zaznamenané žiadne relevantné rozdiely v účinnosti, kvalite či hlásení nežiaducich účinkov medzi originálnymi a biosimilárnymi liekmi. Vývoj biologických liekov je časovo a finančne náročný, čo sa odráža na ich cene – biologické lieky sa radia k najdrahším možnostiam liečby.
Biologická liečba je preto spravidla dostupná len pre úzku skupinu pacientov. Biosimilárne lieky sú lacnejšie než originálne biologické lieky, keďže ich vývoj vychádza z vedeckých poznatkov referenčného lieku. Prispievajú tak ku zlacneniu a sprístupneniu zdravotnej starostlivosti. V žiadnom prípade to však neznamená, že sú menej kvalitné či bezpečné ako originálne biologické lieky.
Jednotlivé kroky ako vzniká biosimilárny liek
Krok č.1 → Vývoj nového (originálneho) biologického lieku výrobcom X. Táto fáza trvá 7 až 10 rokov.
Krok č.2 → Výrobca X môže niekoľko rokov predávať originálny biologický liek ako jediný výrobca. Nazýva sa to patent.
Krok č.3 → Keď vyprší platnosť patentu, iní výrobcovia môžu vyrábať rovnaký druh lieku – tzv. biosimilárny liek.
Krok č.4 → Tak ako pri originálnom biologickom lieku, Európska lieková agentúra aj liekové agentúry jednotlivých štátov posúdia účinnosť a bezpečnosť biosimilárneho lieku
Krok č.5 → Biosimilárny liek je odteraz dostupný pacientom.
Každý pacient sa musí vedieť spoľahnúť na svoj liek. Na tom dennodenne pracuje Štátny ústav pre kontrolu liečiv a celá sieť liekových agentúr v Európskej únii, vrátane Európskej liekovej agentúry.
Ako sa biologicky podobné lieky vyvíjajú a schvaľujú v EÚ?
Európska agentúra pre lieky (EMA) hodnotí biologické lieky vyrobené pomocou biotechnológií vrátane biologicky podobných liekov ešte pred ich schválením a uvedením na trh v EÚ. Povolenie biologicky podobných liekov v EÚ si v porovnaní s ostatnými biologickými liekmi vyžaduje iný súbor údajov. Uplatňujú sa však tie isté vysoké štandardy kvality, bezpečnosti a účinnosti.
Tak, ako pri každom inom lieku, aj pri biologicky podobnom lieku je pred jeho schválením pre uvedenie na trh potrebné preukázať, že jeho prínosy prevažujú riziká. Vyžaduje si to veľké množstvo údajov vrátane údajov týkajúcich sa čistoty a výroby, ako aj správneho fungovania biologicky podobného lieku a tiež rozsiahle porovnanie s referenčným liekom. Porovnania sa vykonávajú postupným spôsobom, ktorý sa začína podrobnými štúdiami v laboratóriu, pri ktorých sa porovnáva štruktúra s funkciou liekov, a následne sa podľa potreby prechádza na porovnávacie klinické štúdie (štúdie na ľuďoch). Po kladnom posúdení zo strany EMA schváli Európska komisia biologicky podobné lieky na používanie u pacientov v EÚ.
Kto rozhoduje o dostupnosti biologicky podobných liekov v jednotlivých krajinách?
Po tom, ako EMA vykoná dôkladné vedecké posúdenie kvality, účinnosti a bezpečnosti biologicky podobných liekov, ich môže Európska komisia schváliť pre uvedenie na trh v EÚ. Ich dostupnosť potom závisí od rozhodnutia spoločnosti uviesť lieky na trh a tiež od orgánu pre lieky a od služieb zdravotnej starostlivosti každej krajiny EÚ.
Ktoré biologicky podobné lieky sú schválené v EÚ?
Všetky biologicky podobné lieky, ktoré sú v súčasnosti schválené v Európskej únii nájdete na stránke European Medicines Agency.
Spracovala a uverejnila: Mária Izakovičová, NCP VaT pri CVTI SR
Zdroj a ďalšie informácie nájdete v dokumentoch:
ŠÚKL: Odpovede na otázky o biologických liekoch
Európska komisia: Čo potrebujem vedieť o biologicky podobných liekoch