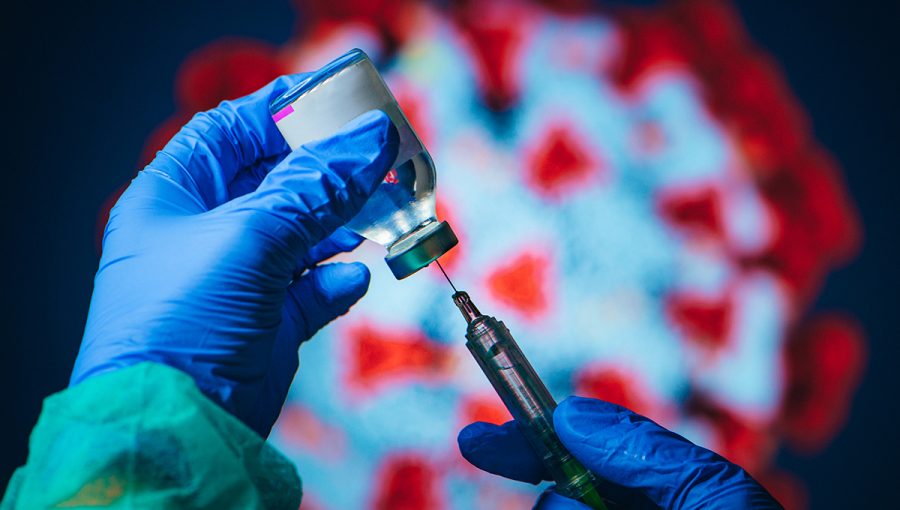
Až keď bude mať o nej všetky potrebné údaje, môže posúdiť, či je vhodné žiadať o jej registráciu.
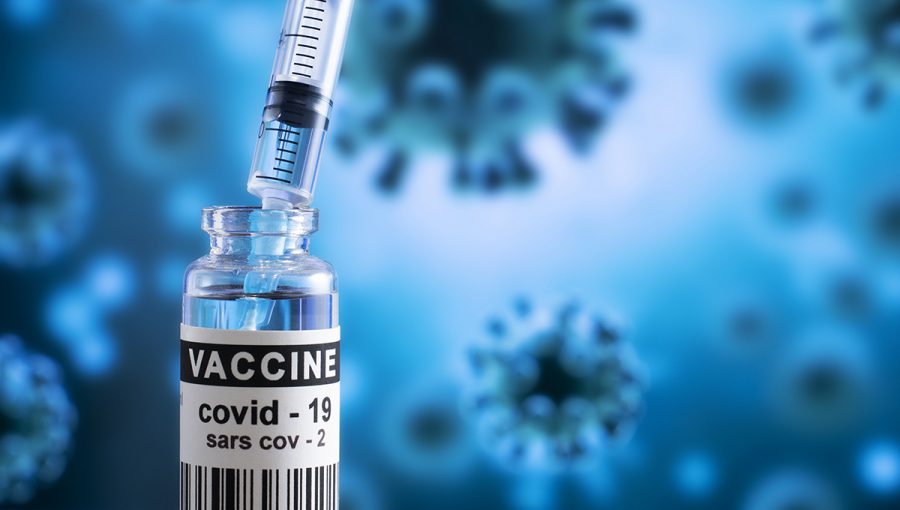
Vakcína proti ochoreniu COVID-19. Zdroj: iStockphoto.com
Pandémia ochorenia COVID-19 sa rozšírila do celého sveta a doteraz má veľmi závažný priebeh i tragické následky. Od jej vypuknutia sa novým koronavírusom vo svete infikovalo takmer 118 miliónov a zomrelo vyše 2,5 milióna ľudí. V Európe sa ním nakazilo vyše 35 miliónov a zomrelo takmer 840 tisíc ľudí. Na Slovensku s ním od 6. marca 2020 bojovalo vyše 323 tisíc ľudí a vyše 8 tisíc z nich zomrelo.
Dodávky očkovacích látok do jednotlivých krajín Európskej únie sú zatiaľ obmedzené, čo ovplyvňuje aj tempo očkovania. Dodnes bolo v EÚ dodaných 51,5 milióna dávok vakcín a podaných 29,2 milióna z nich. Európska komisia sa zasadzuje za zvýšenie kapacity výroby vakcín v priemyselnom odvetví. Zároveň sa zaoberá riešením nových mutácií vírusu s cieľom čo najrýchlejšie vyvinúť a vo veľkom vyrobiť vakcíny, ktoré budú účinkovať aj proti nim.
Vývoj vakcín je kľúčovým riešením zvládnutia pandémie
Vývoj vakcíny obvykle trvá 10 a viac rokov, avšak v takejto krízovej situácii mu nemôžeme venovať toľko času. Vedecké tímy, farmaceutické spoločnosti, výskumné centrá a iné vedecké inštitúcie z celého sveta preto nasmerovali svoje finančné a personálne zdroje tak, aby bola účinná a bezpečná vakcína dostupná v rozsahu 12 až 18 mesiacov.
Takýto cieľ sa dá dosiahnuť iba vtedy, keď prebiehajú súbežne rozsiahle výskumy, klinické skúšania a investície do nových výrobných postupov a zabezpečení surovín. Ide o to, aby sa umožnilo klinické skúšanie s potenciálnou vakcínou a aby sa hneď po tom, ako odborníci schvália, že sa môže uviesť na trh, mohla začať vyrábať vo veľkom.
Napriek tomu, že očkovacie látky proti novému koronavírusu naliehavo potrebujeme, snaha sprístupniť ich rýchlejšie, ako je bežné, vyvolala vo svete nespočetné množstvo otázok a obáv. Odborníci v tejto oblasti však ubezpečujú, že vývoj bezpečnej a účinnej vakcíny v skrátenom časovom rámci neznamená ohrozenie verejnosti, pretože bezpečnosť a účinnosť sú nevyhnutným predpokladom na to, aby ktorákoľvek očkovacia látka dostala povolenie na uvedenie na trh.
Ako sa urýchľuje vývoj vakcín
Pre vývoj očkovacej látky na prevenciu ochorenia COVID-19 sú potrebné výsledky z predklinických a klinických štúdií rovnako ako v prípade iných liekov, avšak v podmienkach núdzovej situácie je možné v zaužívaných plánoch vývoja liekov vykonať isté zmeny. Pracovníci podieľajúci sa na vývoji takýchto vakcín môžu lehoty skrátiť, a to napríklad vykonaním viacerých štúdií naraz a nie postupne.
Potenciálne nové lieky sa testujú najskôr v laboratóriu a následne na dobrovoľníkoch v rámci štúdií, ktoré sa nazývajú klinické skúšania. Tieto testy pomáhajú pochopiť, ako lieky účinkujú, vyhodnotiť ich prínosy a vedľajšie účinky.
Výrobcovia liekov, ktorí si želajú vykonávať klinické skúšanie v EÚ, musia predložiť žiadosti príslušným vnútroštátnym orgánom krajín, v ktorých chcú skúšanie vykonávať. Na úrovni klinického skúšania sa niektoré fázy môžu kombinovať, respektíve zlúčiť. K rýchlejšiemu a plynulému priebehu prispieva aj samotný stav pandémie, ktorý spôsobuje, že v relatívne krátkom čase je možné získať veľký počet testovaných bez toho, aby sa ohrozila kvalita samotných skúšok.
Kto v EÚ zodpovedá za bezpečnosť vakcín
V Európskej únii je za vedecké hodnotenia, dohľad a bezpečnosť liekov vyvinutých farmaceutickými spoločnosťami zodpovedná Európska lieková agentúra (EMA). Agentúra EMA schvaľuje väčšinu inovačných liekov, ktoré sa uvádzajú na trh v Európe. Povolenie vydáva Európska komisia. Až s ním môže spoločnosť uviesť daný liek na trh v celej Európskej únii a Európskom hospodárskom priestore (EHP). O registráciu cez Európsku liekovú agentúru môže požiadať akýkoľvek výrobca z celého sveta.
Registrácia vakcíny cez Európsku liekovú agentúru tiež zaväzuje držiteľa registračného rozhodnutia dodávať ďalšie údaje aj po vydaní registračného rozhodnutia, čím sa zaručuje dlhodobé sledovanie bezpečnosti a účinnosti vakcíny.
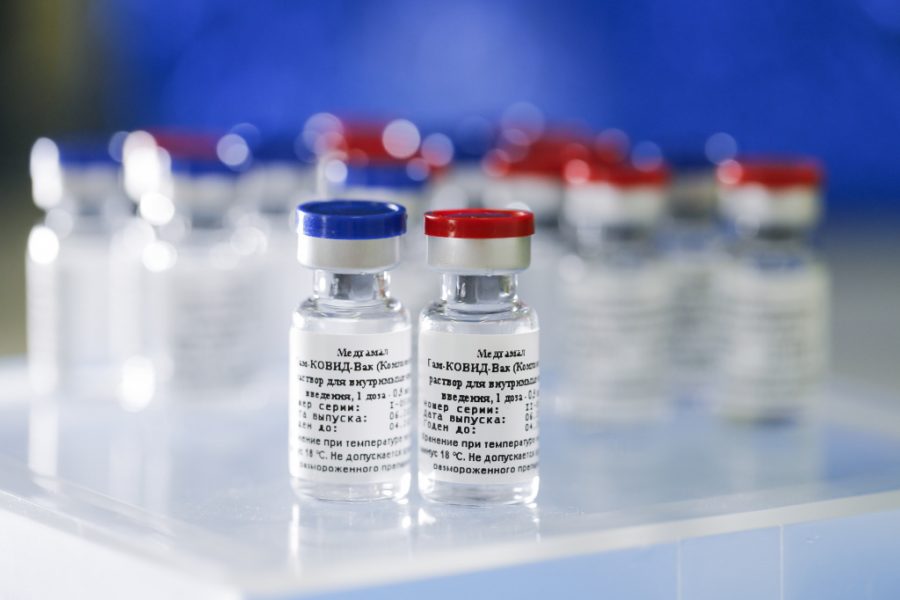
Vakcína Sputnik V. Zdroj: sputnikvaccine.com
Priebežné hodnotenie vakcíny Sputnik V
Európska lieková agentúra (EMA) začala 4. marca 2021 priebežné hodnotenie ruskej vakcíny Sputnik V (Gam-COVID-Vac), ktorú vyvinulo Gamalejovo národné výskumné centrum epidemiológie a mikrobiológie. Žiadateľom v Európskej únii je R-Pharm Germany GmbH.
Začiatok priebežného hodnotenia (takzvané rolling review) je založené na výsledkoch z laboratórnych (predklinických) štúdií a klinických skúšaní a umožňuje ich hodnotenie postupne, teda podľa toho, ako ich žiadateľ dodáva. Až keď má EMA k dispozícii kompletné údaje, môže žiadateľ požiadať o registráciu.
Štúdia uverejnená v renomovanom vedeckom magazíne Lancet naznačuje, že vakcína Sputnik V spúšťa v organizme produkciu protilátok a buniek imunity, ktoré cielia na koronavírus SARS-CoV-2, a môže tak chrániť pred ochorením COVID-19 s účinnosťou až na 92 percent.
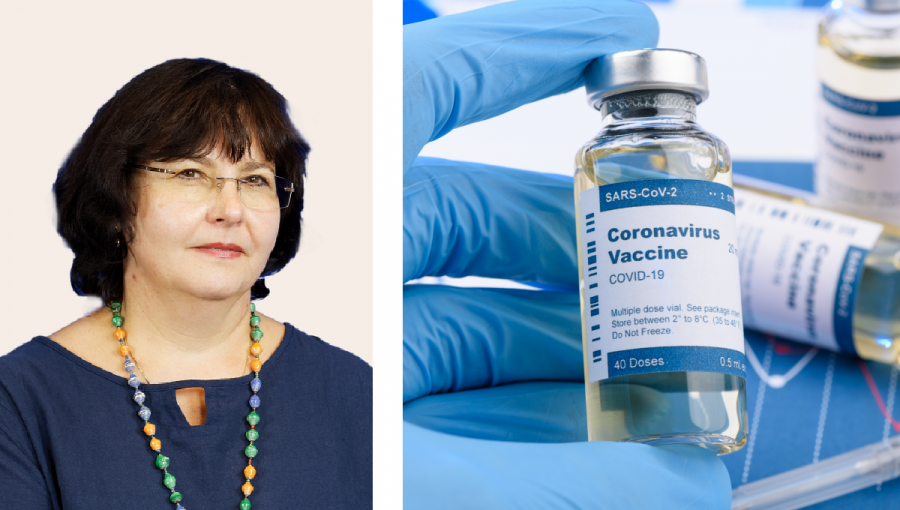
Avšak viacerí vedci upozorňujú, že v nej chýbajú určité údaje. Napríklad aj Norbert Žilka, riaditeľ Neuroimunologického ústavu SAV, v rozhovore na našom portáli pripomína, že je v nej niekoľko drobných nejasností, ktoré je potrebné zodpovedať. Hans-Georg Eichler, vedúci lekár v EMA, v rozhovore pre denník SME je konkrétnejší. Vysvetľuje, že od výrobcu Sputnika V zatiaľ nedostali výsledky rozsiahlych klinických štúdií, ktoré na posúdenie jeho bezpečnosti potrebujú.
ŠÚKL tento postup víta
Európska lieková agentúra vedecky posúdi, či vakcína Sputnik V spĺňa štandardy Európskej únie na účinnosť, bezpečnosť a kvalitu vakcín. Nateraz nie je možné určiť časové lehoty pre registráciu, avšak priebežné hodnotenie proces registrácie významne skracuje.
Stanovisko za Európsku liekovú agentúru vydá vedecký Výbor pre lieky na humánne použitie (CHMP), v ktorom má svojich zástupcov aj Štátny ústav pre kontrolu liečiv – ŠÚKL. ŠÚKL tiež žiada údaje o výrobe a farmaceutickej kvalite v súvislosti s dovozom neregistrovanej vakcíny od výrobcu. Takýto proces je štandardný pre všetky dosiaľ registrované i posudzované vakcíny na prevenciu covidu-19.
Injekčná striekačka a injekčné liekovky naplnené vakcínou. Zdroj: iStockphoto.com
Podľa riaditeľky Štátneho ústavu pre kontrolu liečiv PharmDr. Zuzany Baťovej, PhD., „je začatie priebežného hodnotenia vakcíny Sputnik V na úrovni EMA dobrou správou, ktorá môže smerovať k podaniu žiadosti o registráciu. Takýto postup je v súlade s tým, čo ŠÚKL od začiatku odporúča. Využiť vybudovanú sieť expertov na úrovni EÚ, dodané údaje podrobiť prísnemu vedeckému hodnoteniu a následne očkovať slovenských občanov registrovanou vakcínou.“
Vakcíny na prevenciu proti covidu-19 v EÚ
Na návrh Európskej liekovej agentúry Európska komisia doteraz schválila nasledujúce vakcíny na prevenciu proti ochoreniu COVID-19: BioNTech/Pfizer, Moderna, AstraZeneca a predvčerom aj vakcíny od belgickej firmy Janssen (súčasť koncernu Johnson&Johnson), ktoré by mali prísť na Slovensko v priebehu apríla.
Komisia ukončila prípravné rozhovory s francúzskou spoločnosťou Valneva, ktorej vakcína je ešte stále klinicky testovaná. V priebežnom hodnotení sa nachádzajú aj vakcíny od spoločností CureVac a Novavax. Vo vývoji ďalšej vakcíny spolu pokračujú farmaceutické spoločnosti Sanofi a GlaxoSmithKline. Predpokladajú, že bude dostupná koncom roka 2021.