
Prečítajte si viac o vedkyni
Označenie CRISPR/Cas9 nie je žiadnym tajným kódom, ale názov pre novú, prevratnú metódu molekulárnej biológie a genetiky, pomocou ktorej možno veľmi presne „opravovať“ genetickú informáciu zapísanú v molekule DNA alebo RNA. Podobne, ako sa v žurnalistike texty správ editujú, možno takýmto spôsobom editovať, resp. krisprovať aj gény. Podstata tejto metódy prekvapivo spočíva vo využití imunitného obranného systému baktérií.
Čo vlastne tajomné pojmy CRISPR a Cas9 vyjadrujú?
Pojem CRISPR je skratkou pre zložitý anglický termín „Clustered Regulatory Interspaced Short Palindromic Repeats“, čo preložené do bežnej reči znamená, že ide o úseky prokaryotickej (bakteriálnej) DNA s nahromadenými pravidelne rozmiestnenými krátkymi repetíciami (opakovaniami), ktoré sú prerušované krátkymi úsekmi tzv. spacerovej DNA (t. j. úsekmi nekódujúcej DNA) pochádzajúcej z vírusov. Tie sú „pozostatkom“ predchádzajúcich stretnutí baktérií s vírusmi. (Pripomeňme si, že vírusy môžu baktérie úplne zničiť/lyzovať a použiť ich ako „stavebný materiál“ na tvorbu nových vírusov, alebo sa do nich zabudujú vo forme tzv. profágov a „driemu“ v nich až dovtedy, kým nedostanú povel, aby sa „prebudili“ a bakteriálne bunky zničili.). CRISPR možno prirovnať k očkovaciemu preukazu, do ktorého si baktérie „zapisujú“, s akým vírusom sa už stretli, aby pri nasledujúcej vírusovej infekcii reagovali na ďalšie stretnutie oveľa pohotovejšie a boli voči nej imúnne (odolné). CRISPR možno považovať za určitý rozpoznávací systém vírusovej infekcie, ktorý dokáže infekčný vírus pomocou Cas rozstrihať a začleniť do kruhového bakteriálneho chromozómu v miestach nazývaných CRISPR lokus (miesto). Skratka Cas9 (z angl. CRISPR Associated Protein 9) predstavuje pomenovanie pre enzým – nukleázu, t. j. reprezentanta druhej časti obranného mechanizmu baktérií, ktorý bežne funguje ako „molekulárne nožnice“ a je schopný „strihať“ DNA.

Dve geniálne ženy, ktorým chýba už len Nobelova cena
Geniálna myšlienka, ako strategicky využiť bakteriálne vybavenie na obranu proti votrelcom/vírusom na zámernú manipuláciu s dedičnou informáciou, napadla nezávisle od seba dve vedecké pracovníčky, a to Američanku Jennifer Ann Doudnú a Francúzsku Emmanuelle Marie Charpentierovú.
Obe významné vedecké osobnosti sú držiteľkami mnohých vedeckých vyznamenaní a chýba im už len Nobelova cena. Americká biochemička, profesorka na Kalifornskej univerzite v meste Berkley, J. A. Doudná bola vedúcou osobnosťou pri vývoji CRISPR/Cas9 technológie predurčenej na editovanie genetickej informácie baktérií. Francúzska mikrobiologička, genetička, profesorka a riaditeľka Ústavu Maxa Plancka pre infekčnú biológiu v Berlíne E. M. Charpentierová prispela k odhaleniu úlohy nekódujúcej RNA pri fungovaní CRISPR/Cas9 systému. Obidve vedkyne sa dlhodobo zaoberali štúdiom imunitnej obrany baktérií a keď pred rokom 2012 zistili, že vedecky skúmajú rovnakú problematiku, spojili svoj intelektuálny a vedeckovýskumný potenciál a výsledkom ich spolupráce bol objav techniky CRISPR/Cas9, ktorá využíva bakteriálne enzýmy, kontrolujúce mikrobiálnu imunitu, pri programovateľnom editovaní génov. S novou technológiou oboznámili vedeckú obec prostredníctvom publikácie v prestížnom vedeckom časopise Science v roku 2012. O rok neskôr, ako obidve autorky predstavili svetu prevratnú technológiu, ocenila ich prínos aj vedecká komunita a metóda CRISPR/Cas9 sa dostala do výberu časopisu Science pre objav, ktorý znamenal najväčší prelom roka. Ďalšou významnou osobnosťou, ktorá prispela k využívaniu CRISPR/Cas9 v prospech človeka, ale neskôr aj pri praktickom využívaní pri šľachtení rastlín a živočíchov, je čínsko-americký biochemik, nositeľ veľkého počtu vedeckých ocenení, pracujúci na Massachusettskom Technologickom ústave, profesor Feng Zhang. Profesor biochémie F. Zhang optimalizoval CRISPR/Cas9 systém tak, aby bol vhodný aj pre editovanie ľudských buniek, čím otvoril cestu pre jej praktickú aplikáciu v medicíne.
Enzymatický komplex CRISPR/Cas9 odborníci tiež nazývajú editorom a niektorí nadšenci hovoria o revolučnom nástroji v rukách genetikov, ktorý môže „rozkolísať“ svet. Technika CRISPR/Cas9, vhodná na zámerné zásahy do dedičnej informácie, sa síce začala vyvíjať od roku 2007, avšak oficiálnu premiéru, ako sme už spomenuli, mala vďaka dvom fenomenálnym ženám v roku 2012. Odvtedy sa CRISPR/Cas9 považuje za zázračný nástroj medicíny budúcnosti, ktorý pri editovaní DNA „pracuje“ s chirurgickou presnosťou.
Ako prebieha editovanie/„opravovanie“ génov?
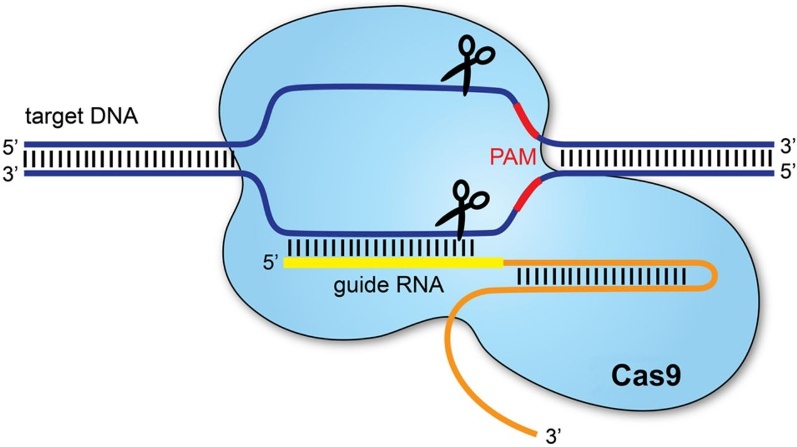
Enzymatický komplex CRISPR/Cas9 sa naviaže na poškodené miesto DNA (sekvenciu nefunkčného génu), vystrihne kus sekvencie a nahradí ju za inú. Vedci dokonca môžu „naprogramovať“ komplex CRISPR/Cas9 tak, aby najprv sám našiel problematickú sekvenciu DNA a narušil ju, alebo aby na určené miesto DNA vniesol cudziu DNA, a tak zámerne „brzdil“, alebo aj „stimuloval“ aktivitu génov. Pomocou krátkeho reťazca, tzv. navádzacej ribonukleovej kyseliny (angl. guide RNA, gRNA) vyhľadá komplex CRISPR/Cas9 poškodené miesto v dedičnej informácii a pomocou „genetických nožníc“ – enzýmu Cas9 ho môže vystrihnúť a vniesť správny gén.
Prečo je editovanie DNA dôležité?
Molekulu ľudskej DNA, nesúcu genetickú informáciu, možno porovnať k veľmi dlhej vete. Pozostáva z 3,2 miliardy „písmen“, resp. základných stavebných kameňov – nukleotidov. V jadre jedinej ľudskej bunky je ukrytá DNA dosahujúca až 2 m. Ak píše človek dlhú vetu, ľahko sa môže pomýliť a urobiť chybu. A to sa občas stáva aj s genetickou informáciou. Dôsledkom ľudskej chyby vo vete, môže byť skutočnosť, že si čitateľ nesprávne vyloží a interpretuje jej význam. Podobný môže byť aj dôsledok chyby, ktorá sa objaví v genetickej informácii. Našťastie je tu jedinečná technika CRISPR/Cas9, ktorá ich dokáže napraviť. Pomocou editovania génov vedci dokážu vystrihnúť z „vety“ – molekuly DNA jedno „slovo“ – sekvenciu predstavujúcu konkrétny gén a preniesť ho inde, prípadne dokážu to „slovo“ z DNA úplne vymazať. Genetický nástroj CRISPR/Cas9 môže teda fungovať, buď ako molekulové nožnice, alebo guma.
Koncom októbra 2017 sa ukázalo, že komplex CRISPR/Cas9 umožňuje vedcom pracovať s genetickou informáciou obsiahnutou v DNA nielen na úrovni „slov“ – sekvencii (kúskov) DNA predstavujúcich gény, ale sa dá využiť aj na modifikáciu jednotlivých „písmen“ – báz DNA. Odborníkom sa podarilo vyvinúť nástroj (v súčasnosti nazývaný CRISPR 2) , ktorý sa nazýva editor báz. Ak sa nachádza akákoľvek zo štyroch báz (adenín – A, guanín – G, cytozín – C a tymín – T) na zlom/nesprávnom mieste „slova“ alebo „vety“, spôsobuje poruchy, ktoré sa môžu prejaviť napr. nejakou dedičnou chorobou. Editor báz umožňuje meniť ich atómovú štruktúru, a tak s bázami manipulovať a zamieňať jednu bázu za druhú.
Spontánne výmeny génov v prírode a v pionierskych časoch génového inžinierstva
Pôvodne sa uskutočňovala výmena génov medzi organizmami toho istého druhu prirodzene v rámci evolúcie, a to väčšinou náhodne. V 90. rokoch 20. storočia sa začali uplatňovať laboratórne techniky genetického inžinierstva, zamerané na tvorbu geneticky modifikovaných organizmov (GMO). Metóda prenosu génov z jedného organizmu na iný, tzv. transgenóza, síce umožnila vsunutie žiadaného génu medzi ostatné gény geneticky upravovaného organizmu, avšak bola nepresná. V pionierskych časoch génového inžinierstva sa síce genetici snažili napraviť chyby prírody, ale často odborníci „triafali naslepo“. Pri génovej terapii sa do nedávna pri „oprave“ poškodeného génu v bunkách človeka postihnutého dedičnou chorobou odborníci nechtiac ocitli v absurdnej situácii, pretože nedokázali presne nahradiť nefunkčný gén za funkčný/nepoškodený. Často ponechali poškodený gén na pôvodnom mieste a k nemu len pridali/prilepili funkčný gén. Nad miestom, kam vsunuli nový gén, tak nemali dostatočnú kontrolu. Mohlo dôjsť aj k tomu, že vnesený gén sa náhodne zabudoval na miesto, kde vážne narušil genetickú informáciu inaktiváciou iných génov (napr. tumor supresorových) alebo aktivoval premenu protoonkogénov na onkogény, a tak vyvolal rakovinu. V roku 2000 napríklad tím francúzskych lekárov oznámil úspešné ukončenie génovej terapie dvanástich chlapcov trpiacich na ťažkú dedičnú nedostatočnosť imunitného systému pomocou prenosu nepoškodeného génu. Chlapcom sa síce imunita obnovila, ale u troch prepukla po niekoľkých rokoch leukémia. Na vine bolo zabudovanie funkčného génu na nesprávne miesto. Občas sa porovnávajú staršie metódy genetického inžinierstva k počítaču, ktorý je potrebné pri spúšťaní nového softwaru prestavať a preinštalovať. Technológia CRISPR/Cas9, ktorú novinári premenovali na CRISPR (podľa toho, ako ju vedci používali v laboratórnom žargóne), možno považovať za génový software. CRISPR sa môže ľahko programovať použitím krátkeho reťazca gRNA. Pomocou technológie CRISPR/Cas9 sa genetické manipulácie posúvajú presnosťou a rýchlosťou na kvalitatívne vyššiu úroveň, pričom sa celý postup modifikácií genómu organizmov podstatne zjednodušuje a zlacňuje, čo je dôležité aj z ekonomického hľadiska.
Prelomové úspechy v medicíne
Technológia CRISPR/Cas9 poskytla ľudstvu veľa fantastických a dovtedy nepredstaviteľných prínosov. Medzi najvýznamnejšie treba spomenúť prenos „zdravej“/nepoškodenej DNA do DNA rakovinových buniek u tzv. beznádejných pacientov, u ktorých klasická liečba rakoviny už nezaberala.
Pravdepodobne najvýznamnejšou terapiou využívajúcou tento nástroj je experimentálna liečba rakoviny prostredníctvom tzv. imunoterapie. CRISPR/Cas9 sa využíva v imunoonkológii pri preprogramovaní imunitných buniek tak, aby rozpoznávali len nádorové bunky a atakovali ich, pričom aby si gény zdravých buniek „nevšímali“.
Medzi úspechy treba zaradiť aj prekvapivú a kontroverznú opravu poškodeného génu realizovanú v Číne priamo v ľudskom embryu. (Poznámka: Takéto experimenty sa samozrejme môžu realizovať len s podmienkou, že sa nesmú ľudské embryá modifikované technológiou CRISPR/Cas9 implantovať do maternice, čo čínski vedci nerešpektujú a obchádzajú). Čínsky vedec Che Ťien-Kchuej zašiel ešte ďalej a tajne bez povolenia a rešpektovania základných etických princípov „vytvoril“ pomocou CRISPR/Cas9 geneticky upravené dvojičky. Na šťastie sú obidve dievčatká zdravé.
Za zmienku stojí aj tvorba umelého/syntetického genómu, pivných kvasiniek Saccharomyces cerevisiae, ktorú možno prirovnať k začiatku cesty vedúcej k „umelému životu“. (Pripomeňme si, že sa doteraz podarilo umelo vytvoriť/syntetizovať len baktériu).
Vedcom sa tiež podarilo pomocou CRISPR/Cas9 vrátiť zrak laboratórnemu potkanovi, ktorý trpel na vrodenú poruchu sietnice.
Prínosom pre medicínu je využitie CRISPR/Cas9 ako tzv. cieleného antibiotika, ktoré zničí len patogénne baktérie vyvolávajúce choroby a ponechá bez poškodenia ostatné baktérie, ktoré sú pre ľudský organizmus prospešné. Tzv. crisprové antibiotiká možno využiť v boji proti baktériám, ktoré sa stali rezistentné na tradičné antibiotiká, napr. akými sú β-laktamové antibiotiká, medzi ktoré patrí aj penicilín.
Využitie CRISPR/Cas9 umožnilo dosiahnuť prelom v boji proti AIDS, pretože sa touto technikou podarilo eliminovať vírus HIV zabudovaný do genetického materiálu napadnutých ľudských buniek. Okrem toho dosiaľ získané výsledky potvrdzujú, že CRISPR/Cas9 predstavuje účinný spôsob ako obmedziť replikáciu herpetických vírusov v ľudských bunkách.
Prínos pre poľnohospodárstvo
Spôsob odstraňovania, pridávania alebo zamieňania úsekov DNA pomocou CRISPR/Cas9 je prísľubom aj pre inovácie v oblasti poľnohospodárstva. Pri porovnávaní s klasickými i modernejšími šľachtiteľskými metódami sa podarilo vo viacerých významných štúdiách potvrdiť, že editovanie DNA je rýchla a lacná metóda vhodná na získavanie kvalitných genotypov nielen pre rastlinnú, ale aj živočíšnu výrobu. Ako nová šľachtiteľská metóda CRISPR/Cas9 zabezpečuje zvyšovanie úrodnosti, odolnosti voči chorobám, tolerancie k suchu, ako aj ďalších parametrov využívaných pri skvalitňovaní poľnohospodárskych plodín. V živočíšnej výrobe sa napr. perspektívne ráta s využitím CRISPR/Cas9 pri získavaní hydiny rezistentnej voči vtáčej chrípke. Pokrok na poli úpravy genetickej informácie rastlín v súčasnosti niektorí odborníci nazývajú „treťou poľnohospodárskou revolúciu“, pričom zdôrazňujú, že technológiu CRISPR/Cas9 možno bezpečne využívať popri existujúcich šľachtiteľských technológiách. CRISPR/Cas9 tiež urýchlila a zjednodušila zámernú tvorbu vybraných transgénnych živočíchov využívaných nielen v poľnohospodárstve, ale aj na výskumné účely pri optimalizácii tzv. modelových organizmov.
Na záver možno konštatovať, že CRISPR/Cas9 dáva genetikom do rúk jedinečný nástroj na opravu dedičnej informácie najrôznejších organizmov, počnúc baktériami, rastlinami a živočíchmi a končiac človekom. Vďaka presnosti CRISPR/Cas9 môžu odborníci eliminovať chyby, ku ktorým dochádzalo pri klasických génových manipuláciách, a tak otvoriť cestu pre nové možnosti manipulovania s génmi v oblasti humánnej medicíny. Keďže táto revolučná metóda predstavuje v súčasnosti najjednoduchší a najlacnejší spôsob, ako zámerne meniť/opravovať DNA, niet pochýb o tom, že editovanie DNA pomocou CRISPR/Cas9 zásadne zmení nielen zdravotníctvo a poľnohospodárstvo, ale možno aj ďalší osud ľudstva.
Autor: prof. RNDr. Eva Miadoková, DrSc. pre redakciu Veda na dosah, Katedra genetiky Prírodovedeckej fakulty Univerzity Komenského v Bratislave
Foto: z archívu prof. RNDr. Evy Miadokovej, DrSc.
Redigovala a uverejnila: VČ



