Bunky, základné funkčné a štruktúrne jednotky všetkých živých organizmov, neustále počas svojho života dozrievajú a zomierajú. Pri bunkovej smrti rozlišujeme 2 typy – nekróza a apoptóza. Pri nekróze bunky v dôsledku vonkajších faktorov, ako je trauma alebo choroba, hynú náhle a nekontrolovane, čo vedie k zápalu postihnutého tkaniva a prípadne napokon aj k jeho poškodeniu. Na druhej strane, apoptóza je geneticky naprogramovaná bunková smrť, pri ktorej nie je vyvolaný žiadny zápal a nedochádza k poškodeniu tkaniva.
Vedci z Ústavu molekulárnej biológie Slovenskej akadémie vied v Bratislave v spolupráci s kolegami z Ústavu hygieny a aplikovanej imunológie Centra pre patofyziológiu, infekciu a imunológiu Viedenskej medicínskej univerzity, odhalili molekulárny mechanizmus, ktorým sú odstraňované mŕtve – apoptotické – bunky prostredníctvom makrofágov, teda špecializovaných buniek imunitného systému.
„Podľa nášho nového článku publikovaného v časopise Journal of Leukocyte Biology produkujú makrofágy po svojom dozretí vyššie množstvo receptora CD222, ktorý potom rozpozná mŕtve bunky špecificky označené plazminogénom – ligandom pre CD222. Znalosť tejto molekulárnej interakcie bude užitočná na hlbšie pochopenie patologických stavov spojených s neúčinným odstraňovaním mŕtvych – apoptotických – buniek, napríklad pri závažných zápalových ochoreniach,“ hovorí vedúci výskumu doktor Vladimír Leksa z Ústavu molekulárnej biológie SAV.
Apoptóza ako taká, je základným fyziologickým procesom, ktorý je kľúčový pri vývine tkanív alebo pri krvotvorbe; čo je dôležité na udržanie homeostázy v tkanivách, a teda aj celkového zdravia. Mŕtve – apoptotické – bunky, ktoré neustále vznikajú, musia ale byť z tkanív okamžite odstraňované makrofágmi v procese fagocytózy nazývanej eferocytóza. Poruchy eferocytózy prispievajú k ťažkým zápalovým ochoreniam alebo autoimunite.

Hlavnú úlohu zohráva podľa vedcov plazminogén, čo je zymogén, ktorý sa podieľa na rozpúšťaní krvných zrazenín.
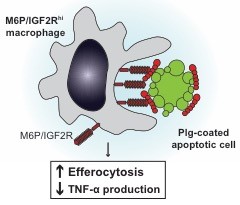
„Okrem toho je však plazminogén dôležitý aj v mnohých iných fyziologických procesoch. Napríklad plazminogén špecificky označuje apoptotické bunky, čo slúži ako signál ´zjedz ma pre makrofágy v tkanivách. V našej novej štúdii sme preukázali, že na povrchu týchto makrofágov sa nachádza receptor pre manózu 6-fosfát (M6P/IGF2R), tiež známy ako CD222, ktorý tento signál na povrchu apoptotických buniek rozpoznáva a sprostredkováva tak odstraňovanie apoptotických buniek,“ hovorí prvá autorka štúdia doktorka Anna Ohraďanová-Repič z viedenského Ústavu hygieny a aplikovanej imunológie.
Výsledky vedcov odhalili doteraz neznámu funkciu receptoru CD222 pri odstraňovaní apoptotických buniek, čo je rozhodujúce pre udržiavanie homeostázy v tkanivách, a teda aj pre zdravie.
„Defekty v odstraňovaní apoptotických buniek môžu viesť k prepuknutiu rôznych porúch, napr. pri chronickej obštrukčnej chorobe pľúc, cystickej fibróze alebo astme. Aj keď bol v našom chápaní toho, ako defektná eferocytóza prispieva k rôznym patologickým stavom, urobený veľký pokrok, je stále nevyhnutné lepšie popísať mechanizmy, ktoré môžu byť zodpovedné za tieto defekty. To napomôže vyvinúť nové terapeutické nástroje nasmerované buď na apoptotické bunky alebo priamo na makrofágy. Jeden z takýchto mechanizmov popisujeme v našom novom článku,“ dodáva doktor Vladimír Leksa.
Spracovala: Monika Hucáková pre portál Veda na dosah
Foto: archív Vladimír Leksa z Ústavu molekulárnej biológie SAV
Uverejnil: LČ








