Na poskladanie celého vesmíru, a teda aj našej Zeme, ktorá je len malým zrnkom v ňom, je treba niečo vyše sto rôznych „základných kameňov“, ktoré voláme chemické prvky. Napríklad základom vzduchu je kyslík a dusík, voda je zložená z kyslíka a vodíka. Vedci predpokladajú, že v jadre našej zemegule je železo a nikel a tiež zistili, že jej kamenný obal obsahuje veľa kremíka a hliníka.
Aj takúto problematiku preberali účastníci Žilinskej detskej univerzity, ktorých privítala Žilinská univerzita v Žiline (UNIZA) vo svojich priestoroch v termíne 9. – 13. júla 2018. Cieľom organizátorov je vzbudiť zvedavosť a záujem detí o objavovanie sveta okolo nich. Štrnásty ročník populárnej Žilinskej detskej univerzity navštívilo 138 detí (77 detí v kurze bakalárik a 61 v kurze inžinierik).
Ako ďalej odznelo v prednáške RNDr. Viery Zatkalíkovej, v lese rastú stromy. „Drevorubači ich zotnú, stolár urobí stôl a málokto objaví v tom stole dub alebo buk. A predsa je to ešte vždy drevo, ktoré je – ako môže chemik v laboratóriu zistiť – najmä z uhlíka, vodíka, kyslíka a dusíka ako všetko živé na Zemi.“
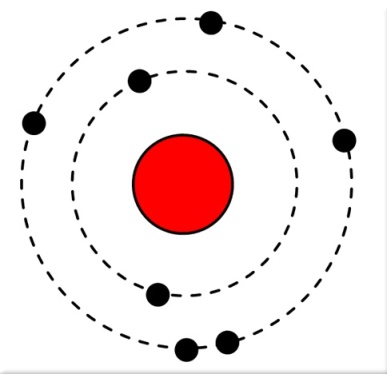
Účastníci detskej univerzity sa dozvedeli, že základnou stavebnou čiastočkou každého chemického prvku je atóm. Je taký maličký, že do bodky by sa vošlo veľa miliónov atómov, čo si ťažko dokážeme predstaviť. A predsa atómy nie sú najmenšími čiastočkami, skladajú sa ešte z menších častíc. V strede majú jadro zložené z protónov a neutrónov, okolo jadra je obal z elektrónov. Protóny a elektróny sú „zelektrizované“ častice. Majú elektrický náboj, protóny kladný (+), elektróny záporný (-). Ale preto, že ich je v atóme rovnaký počet kladných aj záporných, zvonku sa zdá, ako keby nemali elektrický náboj.
Napríklad atómy vodíka majú len jeden protón v jadre, atómy kyslíka majú osem protónov. Všetky atómy toho istého prvku majú rovnaký počet protónov.
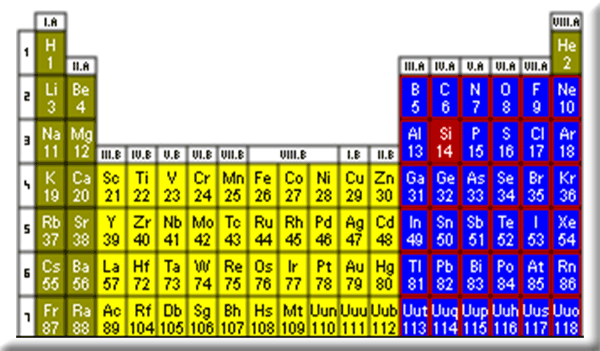
„Keď chemici rozpoznali viacero prvkov, zdalo sa im, že je v nich akýsi neporiadok. Rôzne prvky mali rôzne vlastnosti, ale niektoré zasa podobné. A nebolo jasné, prečo sa niekedy podobajú a niekedy nie. Ale keď chemici ´usporiadali´ známe prvky podľa veľkosti ich atómov, vznikol ´veľký poschodový dom´, ktorý sa nazýva periodická sústava prvkov,“ uviedla prednášajúca.
Pokračovala, že dom má sedem poschodí, ale otočený je akosi naopak. Prvé poschodie je hore, siedme poschodie dole. A viete od čoho závisí ´ubytovanie´ prvkov na jednotlivých poschodiach?, pýtala sa detí. Každý prvok má pridelené poschodie podľa toho, na koľkých vrstvách majú jeho atómy umiestnené svoje elektróny.
„Dom pre prvky má aj osem hlavných vchodov (I. A – VIII. A) a osem vedľajších vchodov (I. B – VIII. B). V tom istom vchode bývajú prvky s podobnými záujmami – podobne sa správajú, často majú podobných kamarátov. A všimli ste si ´menovky na dverách´ jednotlivých prvkov? Majú tam len krátke značky, ale podľa nich ich poznajú na celom svete. Väčšina obyvateľov nášho poschodového domu má veľa kamarátov, ich atómy majú radi spoločnosť. Nájdu sa však aj úplní samotári. Sú to prvky, ktoré bývajú v ôsmom hlavnom vchode periodickej sústavy. Asi by sa aj chceli s niekým kamarátiť, ale nejde to, ich atómy nemôžu nikomu (ani sebe navzájom) ´podať ruku´.“
Príbeh o chudobnom Sodíkovi a bohatom Chlórovi
Deti si ďalej vypočuli príbeh o chudobnom Sodíkovi a bohatom Chlórovi. V siedmom hlavnom vchode poschodového domu pre prvky, na treťom poschodí býval Chlór. Na dverách mal menovku „Cl“. Jeho najväčším bohatstvom bolo sedem elektrónov na tretej, vonkajšej vrstve elektrónového obalu jeho atómov.
Aj keď chlór patril medzi najbohatšie prvky v periodickej sústave, nebol spokojný, lebo bol veľký závistlivec. Celý svoj čas venoval myšlienke, ako získať ešte jeden elektrón, aby sa bohatstvom vyrovnal svojmu susedovi, známemu boháčovi Argónovi. Nevidel inú možnosť ako hľadať po celej periodickej sústave niekoho, od koho by mohol získať chýbajúci elektrón.
Po dlhom hľadaní prišiel Chlór aj do prvého hlavného vchodu a tam na treťom poschodí našiel bývať Sodíka. Každý ho poznal pod značkou „Na“. Sodík bol chudobný, pretože jeho atómy mali na vonkajšej vrstve elektrónového obalu len jeden elektrón.
Napriek svojej chudobe bol však veľmi šľachetný a veľkodušný. Vytušil, že keď daruje Chlórovi svoj jediný elektrón, stanú sa veľké veci … Chlór teda získal Sodíkov elektrón, a tým doplnil svoje aj tak rozsiahle bohatstvo na dlho očakávaný a vysnívaný počet – osem elektrónov.
Lenže v tomto momente sa obaja zmenili. Sodík sa stal kladne nabitým, lebo mu prevyšovali protóny, Chlór záporne nabitým. Takto pozmeneným atómom hovoríme katión a anión. Sodík a Chlór sa stali nerozlučnými priateľmi. Viete, že je to preto, lebo rozdielne elektrické náboje sa navzájom priťahujú. Pri priateľstve katiónu a aniónu chemici hovoria o iónovej väzbe.
Takto sa stal „chemický zázrak“, vypočuli si malí študenti. Z dvoch prvkov Sodíka a Chlóru vznikla chemická zlúčenina NaCl – chlorid sodný (kuchynská soľ), ktorá má celkom iné vlastnosti ako pôvodné látky.
*********************************************
Podujatie Žilinská detská univerzita (ŽDU) organizuje Elektrotechnická fakulta Žilinskej univerzity v Žiline (UNIZA) už od roku 2005, pričom každoročne nadväzuje na výnimočnú aktivitu v oblasti propagácie vedy a techniky v spoločnosti medzi najmladšími žiakmi základných škôl. ŽDU je založená na popularizácii prírodovedných a technických predmetov, hre, interaktivite a tvorivosti, takže základ ostáva rovnaký – pre kurz bakalárik vysvetľovanie prírodných zákonov, jednoduchých princípov a pre kurz inžinierik – aplikácia zákonov do praxe. „UNIZA sa rada aj týmto spôsobom otvára verejnosti. Snažíme sa pritiahnuť deti už od ranného veku k vede a technike, aby v nej objavili krásu a zmysel a mohli ju raz študovať,“ vyjadril sa prof. Ing. Jozef Jandačka, PhD., rektor UNIZA.
Zdroj informácií a fotografií:
https://zdu.uniza.sk/prednasky
Spracovala: Slávka Cigáňová (Habrmanová), NCP VaT pri CVTI SR
Uverejnila: VČ








