
Prečítajte si viac o vedkyni
Ribonukleová kyselina (RNA – z angl. ribonucleic acid) bola v minulosti vedeckou obcou značne podceňovaná „vďaka“ tomu, že mnohé z jej funkcií boli pomerne dlho neznáme, resp. nedostatočne preskúmané. Molekuly RNA boli často vnímané len ako poslíčkovia správ prenášaných od DNA k proteínom. Považovali sa za pasívne súčasti syntézy nových proteínov (t. j. prekladu, resp. translácie genetickej informácie). Títo poslíčkovia iba „niesli“ správy (dedičné informácie zaznamenané v jazyku nukleových kyselín) potrebné na to, aby boli prekladané do jazyka funkčných proteínov nachádzajúcich sa v našich svaloch, obličkách, mozgu, atď.
Aký je rozdiel medzi molekulou DNA a RNA?
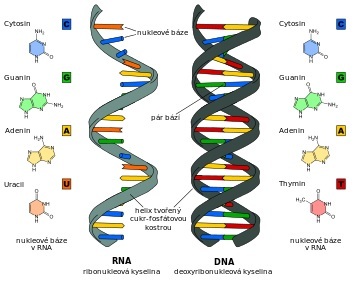 Ribonukleová kyselina sa chemicky líši od „molekuly života“ – DNA len málo. V poradí jej základných stavebných jednotiek sa nachádza namiesto tymínu (T) uracil (U) a cukor deoxyribóza je v RNA nahradený ribózou, pričom je jej sacharidová zložka – ribóza reaktívnejšia než deoxyribóza, a to vďaka prítomnosti voľnej –OH skupiny.
Ribonukleová kyselina sa chemicky líši od „molekuly života“ – DNA len málo. V poradí jej základných stavebných jednotiek sa nachádza namiesto tymínu (T) uracil (U) a cukor deoxyribóza je v RNA nahradený ribózou, pričom je jej sacharidová zložka – ribóza reaktívnejšia než deoxyribóza, a to vďaka prítomnosti voľnej –OH skupiny.
Molekulu RNA môžeme prirovnať k Popoluške, ktorá sa v rozprávke „rozvila do krásy“ a očarila princa. V príbehu, v ktorom hrá hlavnú rolu „RNA – Popoluška“ sa ukázalo, že je pre ľudskú bunku nesmierne dôležitá a že môže v bunke plniť viac veľmi závažných úloh, a to vďaka tomu, že sa v nej nachádza vo viacerých formách/typoch (mediátorová RNA, primerová RNA, transferová RNA, ribozomálna RNA, vírusová RNA, malá jadrová RNA, malá jadierková RNA, malá nekódujúca RNA, malá riadiaca RNA, vaultová RNA, transferovo-informačná RNA, dlhá nekódujúca RNA, atď.). 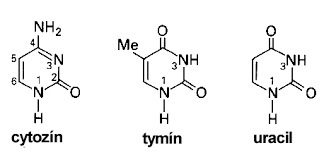 Molekuly RNA sa navzájom odlišujú nielen štruktúrou (poradím základných stavebných tehličiek – báz), priestorovým usporiadaním, ale aj špecifickými funkciami, ktoré vedci postupne odhaľovali. Mnohé z nich sa uplatňujú v procesoch regulácie viacerých biologických procesov, čo prispieva k tomu, že ich prestíž rýchlo rastie. Postupne si predstavíme jednotlivé typy molekúl RNA, pričom začneme tou najznámejšou a skončíme tými, o existencii ktorých bežný čitateľ ani netuší.
Molekuly RNA sa navzájom odlišujú nielen štruktúrou (poradím základných stavebných tehličiek – báz), priestorovým usporiadaním, ale aj špecifickými funkciami, ktoré vedci postupne odhaľovali. Mnohé z nich sa uplatňujú v procesoch regulácie viacerých biologických procesov, čo prispieva k tomu, že ich prestíž rýchlo rastie. Postupne si predstavíme jednotlivé typy molekúl RNA, pričom začneme tou najznámejšou a skončíme tými, o existencii ktorých bežný čitateľ ani netuší.
Mediátorové RNA – RNA sprostredkovateľky
Typ RNA, ktorá prenáša z molekuly DNA genetickú informáciu potrebnú na zaradenie aminokyselín v bielkovine, označujeme dvoma skratkami: mRNA – mediátorová RNA (v anglickom jazyku sa nazýva messenger – posol a má tú istú skratku, t. j. mRNA) alebo iRNA – informačná RNA. Predstavuje 5 – 10 % z celkového množstva molekúl RNA, ktoré sa nachádzajú v ľudskej bunke. Vzniká prepisom (transkripciou) z DNA prebiehajúcim v bunkovom jadre. Po následnej chemickej úprave odohrávajúcej sa bezprostredne po transkripcii, tzv. maturácii pozostávajúcej z viacerých krokov/procesov, z ktorých si pripomenieme predovšetkým jej zostrihanie, presnejšie zostrih (odborne nazývaný splicing), je transportovaná z jadra do cytoplazmy. Tu sa v spojení s ribozómami zúčastňuje syntézy bielkovín. (Ribozómy sú submikroskopické častice prítomné vo všetkých bunkách, na ktorých prebieha syntéza bielkovín). mRNA pozostáva z jedného reťazca. Jej štruktúra a dĺžka závisí od množstva informácií, ktoré nesie.
Primerová RNA
Postupne sa ukázalo, že molekuly RNA sa uplatňujú aj v ďalších procesoch. Fungujú napríklad ako tzv. primery („očká“), t. j. krátke úseky RNA (pozostávajúce z 18 – 22 báz) s voľnou 3′-OH skupinou, ktoré slúžia ako počiatočné miesto replikácie molekuly života – DNA, a tak zohrávajú dôležitú úlohu v procese zdvojenia/replikácie DNA.
Transferové RNA
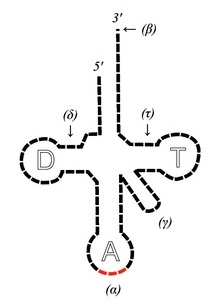 Transferové RNA (tRNA) zasa prenášajú pri syntéze proteínov ich základné stavebné jednotky – aminokyseliny na ribozómy („minifabriky na výrobu bielkovín“), na ktorých podľa inštrukcií mRNA prebieha proteosyntéza. Presnejšie povedané, zabezpečujú prenos/transfer aktivovaných aminokyselín na miesto tvorby novo syntetizovaného bielkovinového reťazca/polypeptidu. Pre molekuly tRNA je charakteristická ich sekundárna štruktúra, ktorá pripomína ďatelinový list.
Transferové RNA (tRNA) zasa prenášajú pri syntéze proteínov ich základné stavebné jednotky – aminokyseliny na ribozómy („minifabriky na výrobu bielkovín“), na ktorých podľa inštrukcií mRNA prebieha proteosyntéza. Presnejšie povedané, zabezpečujú prenos/transfer aktivovaných aminokyselín na miesto tvorby novo syntetizovaného bielkovinového reťazca/polypeptidu. Pre molekuly tRNA je charakteristická ich sekundárna štruktúra, ktorá pripomína ďatelinový list.
Ribozomálne RNA
Ribozomálne RNA (rRNA) predstavujú základnú stavebnú zložku ribozómov. Sú najpočetnejšou skupinou RNA, tvoria až 90 % obsahu nukleových kyselín v bunke. Niektoré časti molekuly rRNA sú lineárne, iné môžu mať tvar dvojitej závitnice. Viete na základe čoho rozdeľujeme rRNA na viac druhov? Molekuly rRNA sa bežne charakterizujú pomocou tzv. sedimentačnej konštanty S. U človeka nachádzame v ribozómoch štyri odlišné typy rRNA, a to 5S rRNA, 5,8S rRNA, 18S rRNA a 28S rRNA. Čím je hodnota S väčšia, tým má rRNA väčšiu molekulovú hmotnosť.
Vírusové RNA
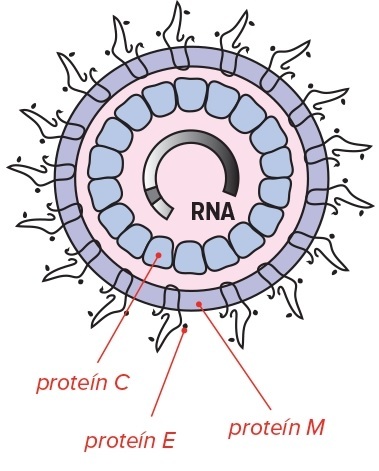
Pri niektorých vírusoch je molekula RNA nositeľom genetickej informácie. Nachádzame ju najmä v rastlinných, ale aj v živočíšnych vírusoch. Pri vírusoch má RNA duálnu funkciu, a to, že slúži ako predloha pre prepis ďalšej molekuly RNA a tiež zastáva aj funkciu mediátora prenášajúceho genetickú informáciu potrebnú pre syntézu proteínov. Väčšinou má jednovláknovú štruktúru, niektoré vírusy však môžu mať aj dvojvláknovú.
Malé jadrové RNA
Malé jadrové RNA (snRNA, z angl. small nuclear RNA) sa podieľajú na procese zostrihu (splicingu) RNA. Sú súčasťou tzv. spliceozómov, t. j. komplexov zložených z viacerých bielkovín a snRNA. Tie pomocou „chemických značiek“ rozpoznajú, ktoré časti z novo syntetizovanej RNA (resp. primárneho transkriptu) nie sú pre danú bielkovinu potrebné a jednoducho ich vystrihnú. Nazývajú sa intróny a predstavujú nekódujúce časti génov. Časti, ktoré sú pre budúcu bielkovinu potrebné, sa nazývajú exóny, resp. kódujúce sekvencie. Po vystrihnutí intrónov sa exóny spoja do reťazca exónov, ktorý vlastne nesie genetickú informáciu a „definuje“ aminokyselinové zloženie budúcej bielkoviny. Pospájané exóny teda tvoria biologicky aktívne molekuly mRNA, ktoré „sú oprávnené“ prenášať genetickú informáciu potrebnú pre zabezpečenie proteosyntézy. Je to proces podobný strihu filmov vo filmových štúdiách. Vo filmovom priemysle sa pri strihaní odstraňujú zo všetkých nasnímaných záberov nevhodné/nekvalitné zábery a nakoniec sa pospájajú tie najvhodnejšie/najkvalitnejšie. Ak by sa intróny z RNA nevystrihli, preklad takejto RNA by sa skončil syntézou nefunkčnej bielkoviny prípadne proteínu, ktorý by bol pre bunku toxický.
O existencii intrónov a exónov a vystrihovaní intrónov sa biológovia dozvedeli v roku 1993, keď bola dvojici Richard J. Roberts a Phillip A. Sharp udelená Nobelova cena za medicínu a fyziológiu. Objav nekódujúcich a kódujúcich sekvencií ovplyvnil celú biológiu. Okrem toho sa ukázalo, že odstraňovanie intrónov a zoraďovanie exónov nemusí vždy prebiehať rovnako. Spliceozóm môže po odstránení intrónov zoradiť exóny v rôznom poradí do viacerých foriem primárnych transkriptov, čo prekvapivo vedie k syntéze rozličných proteínov z rovnakých sekvencií DNA, resp. génov. Tento proces sa nazýva alternatívny splicing a je zdrojom odlišných bielkovín, ktoré pochádzajú z informácie, ktorú nesie tá istá molekula DNA. Aj tu nachádzame paralelu s filmovým zostrihom, keď filmári urobia viac verzií/alternatív filmu, v ktorých nezaradia snímky za sebou v rovnakom poradí.
Alzheimerova choroba ako výsledok straty exónu
Priamy dopad zlyhania niektorého z procesov maturácie RNA, napríklad splicingu na zdravie človeka môžeme demonštrovať na tzv. familiárnej Alzheimerovej demencii s nástupom v skorom veku (okolo tridsiatky). Čo je Alzheimerova choroba? Alzheimerova choroba patrí medzi neurodegeneratívne ochorenia, ktoré sú charakterizované progresívnou a trvalou stratou neurónov v mozgu. Postihnuté sú predovšetkým tie časti mozgu, ktoré zodpovedajú za kognitívne (poznávacie) funkcie. (Syndróm postupného zhoršovania pamäti, myslenia, orientácie, chápania, počítania, kapacity učenia, jazyka a úsudku bez ovplyvnenia vedomia označujeme pojmom demencia). Zmeny kognitívnych vlastností sú často sprevádzané zníženým ovládaním emócií, spoločenského správania a motivácie. Rozoznávame Alzheimerovu chorobu so skorým začiatkom a s neskorým začiatkom. Alzheimerova choroba so skorým začiatkom je obyčajne diagnostikovaná najneskôr pred dosiahnutím 65 rokov života a charakterizuje ju relatívne rýchlo sa zhoršujúci priebeh a výrazné poruchy kognitívnych funkcií. Z génov, ktorých mutácie vedú k Alzheimerovej chorobe v pomerne skorom veku a spôsobujú poruchy tvorby bielkovín si popri géne APP pre amyloidový prekurzorový proteín uveďme gény pre proteíny presenilín 1 – PSEN1 a presenilín 2 – PSEN2. Presenilín je integrálny membránový proteín, ktorý je základnou zložkou enzymatického (gama-sekretázového) komplexu, ktorý katalyzuje štiepenie membránových proteínov, akým je napr. amyloidový prekurzorový proteín. Keďže gén pre presenilín 1 patrí k veľkým génom pozostávajúcim až z desiatich exónov, pri splicingu prvotného prepisu tohto génu môže dôjsť k strate 9. exónu a k nefunkčnej podobe presenilínu 1, čo sa môže prejaviť Alzheimerovou demenciou.
Alzheimerova choroba? Alzheimerova choroba patrí medzi neurodegeneratívne ochorenia, ktoré sú charakterizované progresívnou a trvalou stratou neurónov v mozgu. Postihnuté sú predovšetkým tie časti mozgu, ktoré zodpovedajú za kognitívne (poznávacie) funkcie. (Syndróm postupného zhoršovania pamäti, myslenia, orientácie, chápania, počítania, kapacity učenia, jazyka a úsudku bez ovplyvnenia vedomia označujeme pojmom demencia). Zmeny kognitívnych vlastností sú často sprevádzané zníženým ovládaním emócií, spoločenského správania a motivácie. Rozoznávame Alzheimerovu chorobu so skorým začiatkom a s neskorým začiatkom. Alzheimerova choroba so skorým začiatkom je obyčajne diagnostikovaná najneskôr pred dosiahnutím 65 rokov života a charakterizuje ju relatívne rýchlo sa zhoršujúci priebeh a výrazné poruchy kognitívnych funkcií. Z génov, ktorých mutácie vedú k Alzheimerovej chorobe v pomerne skorom veku a spôsobujú poruchy tvorby bielkovín si popri géne APP pre amyloidový prekurzorový proteín uveďme gény pre proteíny presenilín 1 – PSEN1 a presenilín 2 – PSEN2. Presenilín je integrálny membránový proteín, ktorý je základnou zložkou enzymatického (gama-sekretázového) komplexu, ktorý katalyzuje štiepenie membránových proteínov, akým je napr. amyloidový prekurzorový proteín. Keďže gén pre presenilín 1 patrí k veľkým génom pozostávajúcim až z desiatich exónov, pri splicingu prvotného prepisu tohto génu môže dôjsť k strate 9. exónu a k nefunkčnej podobe presenilínu 1, čo sa môže prejaviť Alzheimerovou demenciou.
Strata exónov pri splicingu veľkých génov vedie aj k autizmu
Ukázalo sa, že narušenie transkripcie génov počas kritických štádií vývoja mozgu dieťaťa v maternici zodpovedá za patológiu a poruchu neurologického vývoja, ako je to aj v prípade autizmu, presnejšie špecifickej oblasti spektra autistických porúch (ASD – Autism Spectrum Disorder), charakterizovaného nedostatočnou spoločenskou komunikáciou, deficitom budovania sociálnych vzťahov, ako aj typickým stereotypným správaním. Porucha má mnoho podôb, stupňov, resp. miery narušenia jednotlivých oblastí. Od uzavretia jedinca v „jeho vlastnom svete“, neschopnosti komunikovať, hrať sa, vnímať a chápať vnemy, ktoré sú pre zdravých ľudí bežné, až po na prvý pohľad zanedbateľné a prehliadnuteľné zvláštnosti v správaní dieťaťa.

V súvislosti s autizmom treba poznamenať, že napriek tomu, že ide o veľmi komplexný fenomén, často pri autizme dochádza buď k mutáciám alebo strate exónov extrémne veľkých génov počas splicingu. Pre zaujímavosť si uvedieme, že tzv. kandidátnymi génmi pre autizmus sú napríklad gény pre synaptické adhézne/priľnavé molekuly: neurexín – Nrxn a neurolignín – NLGN. (Synapsia je miestom styku neurónov alebo neurónu a inej bunky, slúžiace na prenos nervových vzruchov). Neurexín a neurolignín sú dôležité pre synaptické funkcie podobne, ako tzv. shank proteín kódovaný Shank génmi, pri splicingu ktorých môže súčasne vypadnúť aj viac exónov naraz, napríklad exóny č. 4 – 7, exóny č. 13 – 16, alebo sa môžu stratiť len samotné exóny, a to exón č. 9, 11, 21. Prepis a následný preklad takýchto génov vedie k nefunkčnej podobe proteínov, čo sa navonok prejaví príznakmi charakterizujúcimi ASD.
Malé jadierkové RNA
Malé jadierkové RNA (snoRNA, z angl. small nucleolar RNA) hrajú dôležitú úlohu pri syntéze a maturácii molekúl mRNA, rRNA, snRNA a tRNA. Zhluk, resp. klaster snoRNA nachádzajúcich sa na dlhšom ramienku ľudského chromozómu č. 15, participuje na regulácii alternatívneho splicingu. Ukázalo sa, že strata snoRNA nachádzajúcich sa v oblasti ľudského chromozómu (15q11−13) pochádzajúceho od otca vedie k manifestácii Prader-Williho syndrómu. Prader–Williho syndróm (PWS) je vzácna genetická choroba, ktorú charakterizuje nezvládnuteľná chuť na jedlo, malý vzrast a mierna mentálne retardácia. Ľudia s PWS majú poruchu v časti hypotalamu (podlôžka, t. j. spodnej časti medzimozgu tvoriacej dno tretej mozgovej komory), ktorá za normálnych okolností reguluje pocit hladu a sýtosti, a preto sa nikdy necítia sýti.
Malé nekódujúce RNA
Medzi malé nekódujúce RNA – sncRNAs (skratka z angl. small non-coding RNAs) zaraďujeme skupinu krátkych nekódujúcich microRNA (skrátene – miRNA) zväčša o dĺžke 21 – 23 nukleotidov. (Na obrázku je štruktúra týchto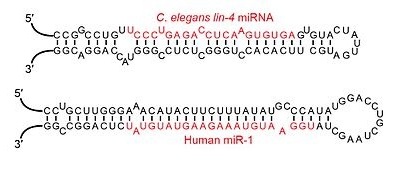 jednovláknových miRNA vyznačená červenou farbou). Prvá miRNA bola identifikovaná v roku 1993 pri pokusoch tímu Victora Ambrosa na červovi Caenorhabditis elegans, u ktorého bol objavený gén, ktorého expresia skončila na úrovni RNA, t. j. transkripcie. Čo je príčinou toho, že sa nejaký gén neprekladá? miRNA má schopnosť naviazať sa na mRNA takéhoto génu, a tým utlmiť, resp. zabrániť jeho ďalšej expresii. V tomto prípade hovoríme o translačnej represii. Hoci bola existencia krátkych RNA známa už niekoľko desaťročí, prikladal sa im význam nanajvýš ako odpadovým produktom. Objavenie ich schopnosti regulovať, napr. potláčať expresiu (prejav) iných génov umožnilo odborníkom vstúpiť do novej éry molekulárnej medicíny. Jednovláknové miRNA disponujú podobne, ako malé dvojvláknové nekódujúce RNA, nazývané malé interferujúce RNA – siRNA (z angl. short interfering RNA) niekoľkými unikátnymi vlastnosťami, ktoré ponúkli dovtedy nové možnosti diagnostiky a terapie mnohých polygénne podmienených ochorení. Ich význam je najmarkantnejší v onkológii, ako aj pri diagnózach závažných neuropsychiatrických porúch. (Mechanizmus utlmovania génovej expresie sprostredkovaný dvojvláknovou RNA s prečnievajúcimi 3´-OH koncami, t. j. siRNA sa nazýva RNA interferencia a označuje sa skratkou RNAi). miRNA a siRNA hrajú významnú úlohu pri regulácii expresie génov zapojených do viacerých dôležitých procesov, napr. bunkovej diferenciácie (špecializácie), proliferácie (delenia), apoptózy (geneticky regulovanej bunkovej smrti) a tumorogenézy (tvorby nádorov).
jednovláknových miRNA vyznačená červenou farbou). Prvá miRNA bola identifikovaná v roku 1993 pri pokusoch tímu Victora Ambrosa na červovi Caenorhabditis elegans, u ktorého bol objavený gén, ktorého expresia skončila na úrovni RNA, t. j. transkripcie. Čo je príčinou toho, že sa nejaký gén neprekladá? miRNA má schopnosť naviazať sa na mRNA takéhoto génu, a tým utlmiť, resp. zabrániť jeho ďalšej expresii. V tomto prípade hovoríme o translačnej represii. Hoci bola existencia krátkych RNA známa už niekoľko desaťročí, prikladal sa im význam nanajvýš ako odpadovým produktom. Objavenie ich schopnosti regulovať, napr. potláčať expresiu (prejav) iných génov umožnilo odborníkom vstúpiť do novej éry molekulárnej medicíny. Jednovláknové miRNA disponujú podobne, ako malé dvojvláknové nekódujúce RNA, nazývané malé interferujúce RNA – siRNA (z angl. short interfering RNA) niekoľkými unikátnymi vlastnosťami, ktoré ponúkli dovtedy nové možnosti diagnostiky a terapie mnohých polygénne podmienených ochorení. Ich význam je najmarkantnejší v onkológii, ako aj pri diagnózach závažných neuropsychiatrických porúch. (Mechanizmus utlmovania génovej expresie sprostredkovaný dvojvláknovou RNA s prečnievajúcimi 3´-OH koncami, t. j. siRNA sa nazýva RNA interferencia a označuje sa skratkou RNAi). miRNA a siRNA hrajú významnú úlohu pri regulácii expresie génov zapojených do viacerých dôležitých procesov, napr. bunkovej diferenciácie (špecializácie), proliferácie (delenia), apoptózy (geneticky regulovanej bunkovej smrti) a tumorogenézy (tvorby nádorov).
Malé riadiace RNA
Malé riadiace RNA (pozostávajúce asi zo 70 báz), ktorých pomenovanie sa najčastejšie vyjadruje skratkou gRNA (z angl. guide RNA), nesú informáciu pre zaujímavý proces, nazývaný editovanie RNA. gRNA je molekula RNA, objavená v mitochondriách, ktorá v komplexe nazývanom editozóm riadi editovanie RNA. Čo je editovanie mRNA? Je to proces patriaci k posttranskripčným úpravám RNA, t. j. je súčasťou maturácie. Podobne ako pri editovaní textu, aj editovaním primárneho transkriptu RNA sa „odstraňujú chyby“, presnejšie doplňujú alebo vynechávajú bázy (písmená) tak, aby mal výsledný „text“ zmysel a po jeho preložení vznikol správny proteín. Pri editovaní dochádza k inzerciám (vkladaniu), deléciam (vypadnutiu) alebo substitúciám (náhrade) báz a výsledkom je „maturovaná“ mRNA. Najčastejšie ide o inzerciu niekoľkých uracilov, alebo blokov uridínu, nahradzovanie cytozínu uracilom a opačne, alebo nahradzovanie adenínu inozínom, prípadne o inzerciu guanínu. Proces editovania spočíva v tom, že mRNA prejde úpravami, pri ktorých sú pôvodné bázy pomocu gRNA nahradené inými. Poradie báz v editovanej mRNA teda už nezodpovedá sekvenciám pôvodného génu/DNA. Podľa editovanej mRNA sa následne syntetizuje proteín, ktorý môže mať úplne inú štruktúru a funkciu. Editovanie RNA je popri alternatívnom splicingu ďalším zdrojom variability, pretože dovoľuje podľa jedného génu syntetizovať viac bielkovín.
Ako prebieha editovanie?
gRNA sa na základe párovania komplementárnych báz viaže s primárnym transkriptom (mRNA) umlčovaného génu pomocou tzv. kotvovej sekvencie. Po naviazaní gRNA na mRNA vstupuje do hry iný úsek gRNA, označovaný ako informačný, ktorý nesie informáciu pre editovanie, resp. dekódovanie informácie prepísanej aj s „chybami“ z DNA. Podľa predlohy (templátu) informačného úseku gRNA, sú do príslušnej časti mRNA postupne vkladané napríklad uridíny a iné z nej vynímané dovtedy, kým sa nestanú obidve sekvencie komplementárne a vznikne medzi nimi dokonalá väzba. Jedna molekula mRNA môže obsahovať veľa „chýb“, preto potrebuje na to, aby bola editovaná viac rôznych gRNA. Editovanie teda prebieha ako kaskáda krokov v presne stanovenom poradí. Naviazanie gRNA1 umožní editovanie len malého úseku mRNA, na ktorý sa po uvoľnení gRNA1 prichytí gRNA2. Tá „odvedie svoju prácu“ a umožní prichytenie gRNA3, atď. Tento proces pokračuje od jedného konca mRNA až po druhý, pričom molekuly gRNA pristupujú k mRNA postupne spolu s komplexom proteínov/enzýmov vo forme tzv. editozómu, ktorý je priamym realizátorom zmien. Popri mRNA je editovaná aj tRNA, ktorá by bez editovania nemohla zaujať správnu priestorovú štruktúru (ďatelinového listu).
Vaultové RNA
Vaultová RNA (vRNA) bola objavená ako súčasť RNA-proteínových častíc, ktoré pozostávajú z hlavného proteínu (MVP), dvoch malých proteínov (VPARP a TEP1) a viacerých malých netranslatovaných (neprekladaných) molekúl RNA. Nachádzajú sa na povrchu jadrovej membrány a sú spojené so systémom jadrových pórov. Molekuly vRNA sú veľmi konzervatívne, čo sa prejavuje najmä ich priestorovou štruktúrou. Tieto molekuly RNA sú výsledkom transkripcie realizovanej RNA polymerázou III. Predpokladá sa, že zohrávajú úlohu v procesoch intracelulárneho (vnútrobunkového) a nukleocytoplazmatického (prebiehajúceho medzi jadrom a cytoplazmou) transportu látok. Podarilo sa dokázať, že vRNA síce nemá vplyv na štruktúru jadrovej membrány, avšak isto ovplyvňuje jej funkciu.
Transferovo-informačné RNA
Transferovo-informačná – tmRNA (z angl. transfer-messenger RNA) bola nájdená v baktériách i v mitochondriách plesní. Názov transferovo-informačná získala vďaka duálnej funkcii, t. j. funguje jednak ako tRNA a jednak ako iRNA/mRNA. Predstavuje unikátnu molekulu, ktorá sa zúčastňuje na procese nazývanom trans-translácia (raws-translation). Keď v procese proteosyntézy nasadne ribozóm na poškodenú mRNA, „má problém“ s jej prekladom a zastaví sa. Nedokončený peptidový reťazec by mohol byť pre bunky nebezpečný, a preto „zasahuje“ tmRNA. K ribozómu sa najprv naviaže ako tRNA a následne je ribozómom „preložená“ ako mRNA. Okrem toho tmRNA kóduje krátky polypeptid slúžiaci ako značka na degradáciu nedokončeného proteínu. Súčasne práve ona zaisťuje aj degradáciu poškodenej mRNA a uvoľňuje ribozóm.
Dlhé nekódujúce RNA
Dlhá nekódujúca molekula RNA – lnc RNA (z angl. long non-coding RNA) predstavuje molekuly RNA, ktoré fungujú ako regulátory expresie génov a modulátory neurálnej funkcie. Môžu ovplyvniť neurodegeneráciu, t. j. poškodzovanie nervových štruktúr vedúcich k strate neurologických funkcií. Existuje celý rad mechanizmov, prostredníctvom ktorých môžu lncRNA ovplyvňovať génovú expresiu. Molekuly lncRNA môžeme všeobecne definovať ako nekódujúce transkripty – prepisy genetickej informácie z DNA do molekúl RNA pozostávajúcich aspoň z 200 stavebných jednotiek (ribonukleotidov). Mnohé lncRNA sú vlastne nerozlíšiteľné od mRNA. Z DNA sú prepisované podobne ako molekuly mRNA enzýmom RNA-polymeráza II a prekvapivo tvoria väčšinu RNA molekúl prítomných v cicavčích bunkách.
Molekula RNA sa vďaka pokroku vo vede premenila zo zaznávanej Popolušky na molekulu, resp. celú škálu molekúl RNA, ktoré sprostredkovávajú pre bunku esenciálne a donedávna ešte neodhalené funkcie. Skončila sa tým „dráma“ nedoceňovania tejto úžasnej molekuly. Vedci napríklad postupne začínajú zbavovať skupinu malých neprekladaných molekúl ich tajomstiev, predovšetkým odhaľovaním ich úlohy v procesoch regulácie génovej expresie. Zdá sa, že tieto molekuly hrajú kľúčovú rolu pri celom rade chorôb, vrátane kardiovaskulárnych. So zvyšujúcou úrovňou poznania sa odborníkom otvárajú nové postupy, pri ktorých sa snažia využiť tieto malé molekuly v klinickej praxi, a to nielen v diagnostike, ale i pri terapeutických postupoch. Začala sa písať nová a trochu prehnane vyjadrené až oslavná etapa príbehu jednej z nukleových kyselín.
Autor: prof. RNDr. Eva Miadoková, DrSc. pre redakciu Veda na dosah, Katedra genetiky Prírodovedeckej fakulty Univerzity Komenského v Bratislave
Foto v článku: z archívu prof. RNDr. Evy Miadokovej, DrSc.
Úvodné foto: Pixabay.com /PublicDomainPictures/
Redigovala a uverejnila: VČ



