Európska lieková agentúra (EMA) a jej Výbor pre lieky na humánne použitie (CHMP) začali „priebežné hodnotenie“ dostupných údajov k trom vakcínam proti vírusu SARS-CoV-2.

Rozhodnutie začať so zrýchleným hodnotením je založené na predbežných výsledkoch predklinických štúdií. Viac v rozhovore prezradil z Centra experimentálnej medicíny Slovenskej akadémie vied a Štátneho ústavu pre kontrolu liečiv. V EMA je zároveň súčasťou procesu vedeckého odporúčania pre registráciu vakcín na prevenciu ochorenia COVID-19.
Aké sú najnovšie poznatky o vakcínach proti novému koronavírusu, ktoré máme aktuálne k dispozícii?
Doteraz získané výsledky naznačujú, že vakcíny spúšťajú produkciu protilátok a vyvolávajú odpoveď T buniek (bunky imunitného systému, ktoré vytvárajú špecifickú obranu tela). Posudzovací proces však ešte prebieha a na definitívne závery si budeme musieť ešte počkať. Keďže máme svojich zástupcov vo vedeckých výboroch EMA, máme aj všetky potrebné informácie o procese schvaľovania vakcín, ktoré vstupujú na náš trh.
EMA skrátila proces registrácie nových liekov proti ochoreniu COVID-19, a teda aj vakcín. Ako takýto proces funguje?
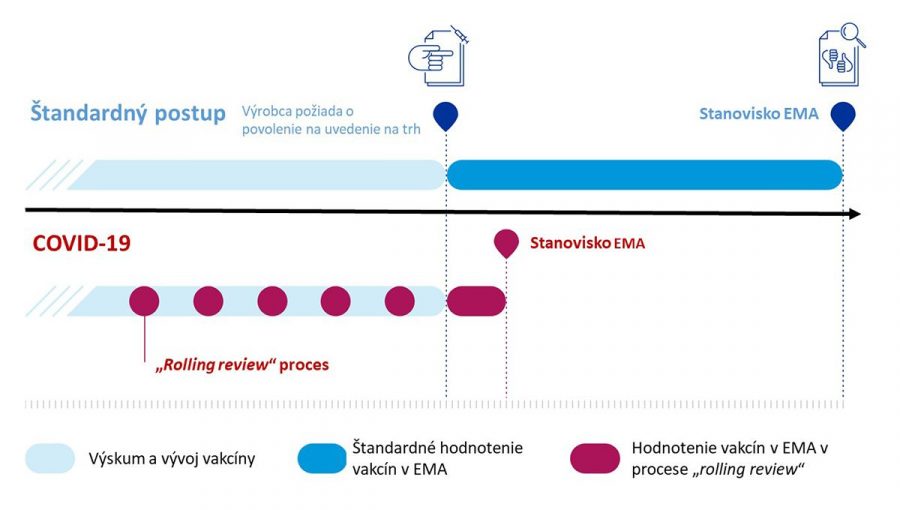
Tento spôsob sa volá priebežné hodnotenie alebo rolling review. Je jedným z regulačných nástrojov, ktoré EMA používa na urýchlenie posúdenia lieku alebo vakcíny počas výnimočného stavu ohrozenia verejného zdravia občanov EÚ. Za normálnych okolností musia byť všetky údaje o účinnosti, bezpečnosti a kvalite lieku i vakcíny predložené pred začiatkom posudzovania vo formálnej žiadosti o povolenie na uvedenie na trh. V prípade tzv. rolling review Výbor pre lieky na humánne použitie (CHMP) v EMA už posudzuje údaje priebežne tak, ako sú k dispozícii z prebiehajúcich in vivo a in vitro štúdií, pred formálnym podaním žiadosti o registráciu. Akonáhle výbor rozhodne, že predložené údaje sú dostatočné a zodpovedajú aktuálnej vedeckej a regulačnej kvalite, žiadateľ predloží formálnu žiadosť o registráciu. Prehodnotením všetkých údajov môžu členovia výboru dospieť k stanovisku, či liek alebo vakcína môže byť odporúčaný/odporúčaná na registráciu alebo nie. Vždy platí, že vyhodnotenie pomeru prínosov a rizík musí byť v prospech prínosu v boji proti nákaze.
Aké sú kľúčové vedecké zásady požadované na vakcíny proti ochoreniu COVID-19?
Vzhľadom na globálny charakter pandémie a potrebu zabezpečiť, aby všetci, čo vyvíjajú vakcíny, generovali vždy spoľahlivé výsledky, ktoré zodpovedajú potrebám regulačných orgánov na celom svete, sa EMA a Medzinárodné regulačné orgány pre lieky (ICMRA) dohodli počas tohto leta na hlavných zásadách k návrhom klinických štúdií fázy III s vakcínami proti ochoreniu COVID-19. Fáza III je posledným štádiom testovania pred tým, než sa môže predložiť žiadosť o registráciu vakcíny (a liekov) regulačnému orgánu. Klinické štúdie fázy III sa zameriavajú hlavne na preukázanie účinnosti a bezpečnosti vakcíny na desať tisíckach dobrovoľníkov. To, či sa vakcína odporučí na registráciu, sa však posudzuje od prípadu k prípadu na základe všetkých dostupných údajov o jej bezpečnosti, účinnosti a kvalite.
Ako sa od seba jednotlivé vakcíny líšia?
Jednoducho povedané, odlišnosť vakcín by som rozdelil na dva typy. Jednak je to rozdiel vo výrobnom procese a tiež obsahu účinnej látky vo vakcíne samotnej. Výrobcovia vakcín a vedci používajú zavedené výrobné systémy, ktoré sa v súčasnosti používajú pre bezpečné a účinné vakcíny. Okrem toho neustále skúmajú nové prístupy k výrobe a vývoju vakcín. Niektoré z doterajších poznatkov sa teda uplatňujú aj pri vývoji vakcín proti SARS-CoV-2.
Je to tak, že od vakcín, ktoré sa vyvíjajú pomocou nových metód, sa očakáva zvýšenie objemu a rýchlosti výroby v porovnaní s inými typmi vakcín?
Áno, a tiež sa očakáva zvýšenie stability produktu a vyvolanie adekvátnej imunitnej reakcie. Ostatné vakcíny sa vyvíjajú pomocou už existujúcich metód, čo je tiež výhodné. Tie sa používajú aj pri vakcínach proti iným chorobám, čo znamená, že by sa mohli využiť terajšie výrobné zariadenia na produkciu vakcín proti SARS-CoV-2 vo väčšom rozsahu.
Ako je to s vakcínami, ktoré sa potom odlišujú obsahom, teda mechanizmom, akým pôsobia na imunitný systém?
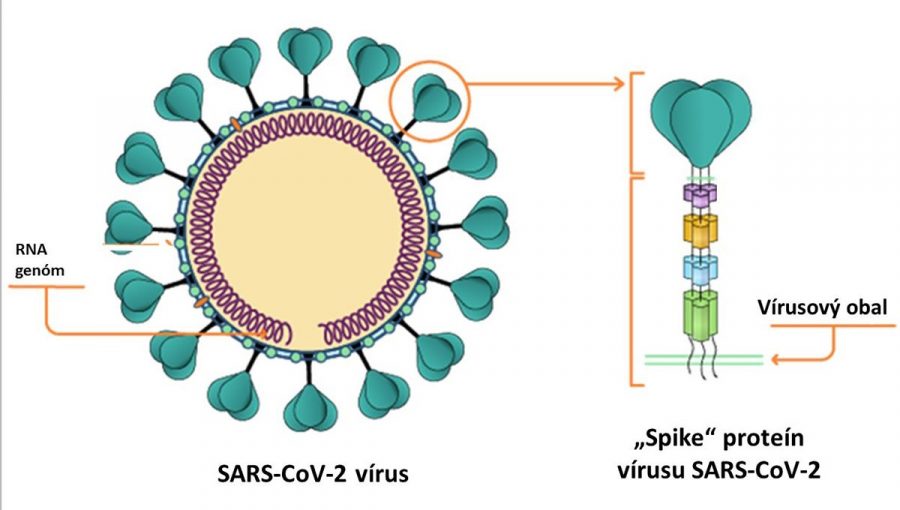
Pokiaľ ide o mechanizmus vyvolávajúci imunitnú odpoveď, tak v súčasnosti prebieha v EMA hodnotenie troch vakcín, ktoré sa líšia účinnou látkou. Prvý typ je vakcína od výrobcu AstraZeneca v kooperácii s Oxfordskou univerzitou a je známa ako Oxfordská. Očakáva sa, že Oxfordská vakcína bude účinkovať tak, že pripraví telo na obranu proti infekcii SARS-CoV-2. Vírus totiž využíva na svojom vonkajšom povrchu proteíny, ktoré sa nazývajú spike proteíny, a tie sú potrebné na vstup do buniek tela a vyvolanie ochorenia COVID-19. Táto vakcína obsahuje vírus, ktorý je z rodiny adenovírusov a ktorý bol upravený tak, aby obsahoval gén na tvorbu spomínaného spike proteínu SARS-CoV-2. Samotný adenovírus je upravený takým spôsobom, že sa nedokáže množiť a nespôsobuje ochorenie.
Ďalším typom vakcíny je vakcína od výrobcu BioNTech v spolupráci so spoločnosťou Pfizer. Táto vakcína obsahuje mRNA, na základe ktorej sa vytvorí spike proteín. Keďže molekula mRNA je veľmi citlivá a ľahko sa rozkladá, vo vakcíne je pokrytá malými tukovými časticami, ktoré zvyšujú jej stabilitu.
Rovnakým spôsobom na princípe mRNA účinkuje aj tretia vakcína. Je od výrobcu Moderna Biotech Spain, S. L. Spoločným výsledným efektom všetkých troch vakcín je to, že imunitný systém človeka sa s obsahom vakcíny vysporiada proti týmto aktívnym zložkám vytváraním prirodzených obranných látok a primeranou odpoveďou T buniek. Ak neskôr očkovaná osoba príde do styku s novým koronavírusom, imunitný systém už rozpozná vírus a je pripravený na jeho zneškodnenie, čím sa človek pomáha chrániť pred ochorením COVID-19.
Vznikli aj pochybnosti, aké bezpečné budú vakcíny proti ochoreniu COVID-19. Ako sa monitoruje bezpečnosť týkajúca sa nežiaducich účinkov vakcíny ako takých?
Vedecké hodnotenie akejkoľvek vakcíny v EÚ musí v každej situácii preukázať, že prínos vakcíny v ochrane ľudí je oveľa väčší ako akékoľvek potenciálne riziko. V čase schválenia pochádza hlavný súbor dát o bezpečnosti a účinnosti vakcín z rozsiahlych klinických štúdií. Dobrovoľníci sú náhodne priradení do skupiny, ktorá dostáva skúšanú vakcínu, a skupiny, ktorá dostáva placebo. Takto je umožnené sledovať bezpečnosť a účinnosť skúmanej vakcíny za kontrolovaných podmienok v súlade s prísnymi protokolmi a smernicami EÚ. Tento prístup sa aplikuje vždy, nehľadiac na rýchlosť procesu schvaľovania. Po úspešnom schválení dostane vakcínu oveľa väčší počet ľudí ako počas klinického skúšania. Právne predpisy EÚ požadujú, aby sa bezpečnosť vakcín sledovala aj po registrácii. V súčasnosti s istotou ešte nevieme, aké sú dlhodobé následky po prekonaní ochorenia COVID-19. Nesmierne dôležité je rozlíšiť samotný nežiaduci účinok liečby a dlhodobé následky ochorenia COVID-19. Tento fakt sa bude musieť intenzívne skúmať, aby lekári vedeli identifikovať a klasifikovať práve špecifické prejavy jedného či druhého. Na tento účel sú podávané aj vedecké granty na SAV, ktorých cieľom by mal byť výskum dlhodobých následkov ochorenia COVID-19. Každý jednotlivec po očkovaní môže prispieť tým, že využije rôzne spôsoby hlásenia nežiaducich účinkov, ak sa prejavia. Podľa mňa najjednoduchším spôsobom je oznámenie svojmu ošetrujúcemu lekárovi, ktorý stav svojho pacienta pozná, a vie tak poskytnúť cenné údaje Štátnemu ústavu pre kontrolu liečiv na analýzu. Pacient tiež môže hlásiť podozrenia na nežiaduce účinky priamo ŠÚKL-u.










