
Prečítajte si viac o vedkyni
Genetici považujú rakovinu za chorobu génov, presnejšie za skupinu ochorení spôsobených mutáciami génov a zásahom do prejavu (expresie t. j. transkripcie a translácie) génov.
Výsledkom vzniku mutácií v tzv. tumor-supresorových génoch, protoonkogénoch a mutátorových génoch regulujúcich rast a delenie buniek je strata kontroly bunkového delenia (proliferácie), pretože sa v bunkách viac neplnia kontrolné úlohy, ktoré sú bežne zabezpečované v zdravých bunkách. Neregulované a neobmedzené delenie buniek vedie k vzniku nádorov (tumorov). Nádory sú výsledkom genetických porúch – mutácií, ktoré môžu vyvolať (indukovať) faktory životného prostredia, napr. pesticídy, kozmetické prípravky, potravinové stabilizátory, farmaceutické prípravky, atď. Okrem spomenutých chemických látok, resp. chemických karcinogénov, nádory môžu vyvolať aj fyzikálne faktory, napr. rôzne typy žiarenia (RTG, UV) alebo biologické agensy, napr. vírusy. K vzniku nádorov prispievajú aj faktory, ktoré ovplyvňujú samotnú expresiu vyššie uvedených génov. U niektorých typov nádorov je známa ich genetická predispozícia, „vďaka“ ktorej sa zvyšuje pravdepodobnosť, že sa u človeka s dedičnou predispozíciou nádor objaví.
Každý nádor však neznamená automaticky rakovinu. Nádory môžu byť nezhubné (benígne), napr. bradavice, materské znamienka, atď. alebo v tom horšom prípade zhubné (malígne, rakovina). Obidve skupiny sa vyznačujú charakteristickými znakmi pozorovateľnými voľným okom, ale predovšetkým mikroskopicky. K charakteristickým a voľným okom pozorovateľným znakom benígnych nádorov patrí ich pomerne dobrá ohraničenosť, pomalý rast a menší rozmer, zatiaľ čo malígne nádory sú nepravidelne ohraničené, pomerne rýchlo rastúce a často i väčšie. V súčasnosti je známych viac ako 100 druhov rakoviny, ktoré sú zvyčajne pomenované podľa orgánu, tkaniva, alebo typu postihnutých buniek. Nádory, ktoré vznikajú na rovnakom mieste, ale líšia sa tým, či sú zhubné alebo nezhubné, majú rôzne mená.
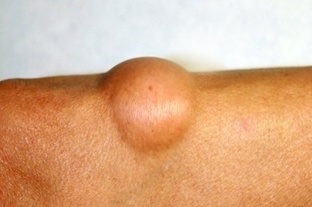 Napríklad benígny nádor z tukového väziva sa nazýva lipóm, jeho malígny variant liposarkóm. Okrem tzv. solídnych (pevných) nádorov poznáme aj leukémie, čiže difúzne nádorové ochorenia krvi a kostnej drene. Zhubné solídne tumory vznikajú na jednom mieste niektorého z orgánov, kým v prípade leukémií krvné nádorové bunky cirkulujú po celom tele. Väčšinu pevných nádorov je možno odstrániť chirurgicky, chemoterapiou alebo kombinovanou terapiou. Neliečený nádor môže mať pre človeka fatálne dôsledky, najmä vtedy, ak sa pevné zhubné nádory šíria ďalej do rôznych časti organizmu a tvoria sekundárne nádory. Takéto procesy nazývame metastázovanie. Názov pochádza z gréčtiny a znamená zmenu stavu. S rastúcim vekom stúpa riziko výskytu rakoviny.
Napríklad benígny nádor z tukového väziva sa nazýva lipóm, jeho malígny variant liposarkóm. Okrem tzv. solídnych (pevných) nádorov poznáme aj leukémie, čiže difúzne nádorové ochorenia krvi a kostnej drene. Zhubné solídne tumory vznikajú na jednom mieste niektorého z orgánov, kým v prípade leukémií krvné nádorové bunky cirkulujú po celom tele. Väčšinu pevných nádorov je možno odstrániť chirurgicky, chemoterapiou alebo kombinovanou terapiou. Neliečený nádor môže mať pre človeka fatálne dôsledky, najmä vtedy, ak sa pevné zhubné nádory šíria ďalej do rôznych časti organizmu a tvoria sekundárne nádory. Takéto procesy nazývame metastázovanie. Názov pochádza z gréčtiny a znamená zmenu stavu. S rastúcim vekom stúpa riziko výskytu rakoviny.
Čo sú tumor-supresorové gény?
Tumor-supresorové gény (pomenované tiež antionkogény alebo recesívne onkogény) kódujú, resp. zodpovedajú za syntézu bielkovín, ktoré chránia zdravú bunku pred nekontrolovateľným delením a nádorovú bunku zasa dokážu prinútiť k samovražde. Proteíny kódované tumor-supresorovými génmi majú teda antiproliferačný účinok (t. j. zabraňujú neregulovanému deleniu nádorových buniek), podporujú diferenciáciu (funkčnú špecializáciu) buniek, opravu mutáciou poškodenú DNA a apoptózu (geneticky regulovanú bunkovú samovraždu). Tumor-supresorové gény sú výnimočné gény, ktoré dokážu zabrániť nádorovým ochoreniam. Mutácie, ktoré spôsobujú inaktiváciu antionkogénov, hrajú zásadnú úlohu v procese karcinogenézy, pretože v konečnom dôsledku vyvolávajú malígny zvrat bunky, resp. ju menia na nádorovú. Povedané inými slovami, v takýchto bunkách funkčne „zlyhal“ tumor-supresorový gén. V každej somatickej (telovej) bunke sa nachádza asi 40 tumor-supresorových génov. Na to, aby sa stali tumorogénne, musia mutovať ich obidve alely (t. j. dve formy génu zodpovedné za ten istý znak/vlastnosť, ktoré dieťa zdedí od oboch rodičov). Dieťa môže zdediť od každého z rodičov dominantnú alelu. Vtedy sa stáva dominantným homozygotom. Môže tiež od jedného rodiča zdediť dominantnú alelu a od druhého recesívnu alelu, vtedy je tzv. dominantným heterozygotom, u ktorého sa funkčne prejaví len dominantná alela. Ak od obidvoch rodičov zdedí recesívnu alelu, je recesívnym homozygotom, u ktorého sa dominantná alela nemôže prejaviť. Alely tumor-supresorových génov sa môžu mutáciami zmeniť z dominantných (ktoré suprimujú/potláčajú vznik nádorov) na recesívne (pri ktorých sa v homozyotnom stave tvoria nádory).
Prvý tumor-supresorový gén
Ako prvý bol objavený tumor-supresorový gén, ktorý bol nazvaný retinoblastomový gén (v odbornej literatúre označovaný skratkou Rb) a zodpovedal za syntézu tzv. retinoblastómového proteínu (RB-proteín). Vyskytuje sa 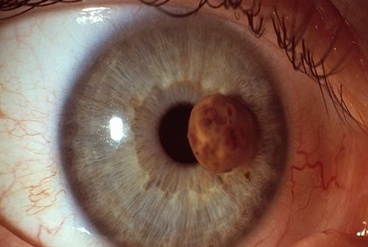 v každej ľudskej bunke, kde reguluje bunkový cyklus. Retinoblastomový gén (Rb) a další tumor-supresorový gén TP53, kódujúci proteín p53, fungujú ako „brzdy“ bunkového delenia. Ak obidve alely Rb génu mutujú (menia sa na recesívne), vzniká nádor oka (retinoblastóm). S ním súvisí tzv. dvojzásahová teória, ktorú v roku 1971 formuloval Alfréd Knudson, keď objasnil vznik vzácneho hereditárneho (dedičného) nádoru oka – retinoblastómu. Na rozdiel od častejšie sa vyskytujúceho tzv. sporadického retinoblastómu, ktorý vzniká v dôsledku dvoch náhodných mutácií obidvoch aliel Rb génu v bunkách sietnice, pri dedičnej forme jednu mutovanú alelu zdedí jej nositeľ od jedného z rodičov, a tým aj predispozíciu na retinoblastóm. Ich dieťa je po narodení heterozygot, pretože v jeho bunkách sa nachádza jedna dominantná, t. j. funkčná alela Rb génu, ktorá zabraňuje vzniku nádoru a druhá recesívna, nefunkčná alela. Vďaka prítomnosti dominantnej alely Rb génu sa u dieťaťa (heterozygota) nádorová predispozícia zdedená po jednom z rodičov najprv neprejavuje. Ak však u takéhoto dieťaťa dôjde k náhodnej mutácií a funkčnej eliminácii aj druhej alely Rb génu, v bunkách sietnice dieťaťa sa začne tvoriť nádor. Tento proces sa odborne nazýva strata heterozygotnosti a označuje sa skratkou LOH (z angl. loss of heterozygozity).
v každej ľudskej bunke, kde reguluje bunkový cyklus. Retinoblastomový gén (Rb) a další tumor-supresorový gén TP53, kódujúci proteín p53, fungujú ako „brzdy“ bunkového delenia. Ak obidve alely Rb génu mutujú (menia sa na recesívne), vzniká nádor oka (retinoblastóm). S ním súvisí tzv. dvojzásahová teória, ktorú v roku 1971 formuloval Alfréd Knudson, keď objasnil vznik vzácneho hereditárneho (dedičného) nádoru oka – retinoblastómu. Na rozdiel od častejšie sa vyskytujúceho tzv. sporadického retinoblastómu, ktorý vzniká v dôsledku dvoch náhodných mutácií obidvoch aliel Rb génu v bunkách sietnice, pri dedičnej forme jednu mutovanú alelu zdedí jej nositeľ od jedného z rodičov, a tým aj predispozíciu na retinoblastóm. Ich dieťa je po narodení heterozygot, pretože v jeho bunkách sa nachádza jedna dominantná, t. j. funkčná alela Rb génu, ktorá zabraňuje vzniku nádoru a druhá recesívna, nefunkčná alela. Vďaka prítomnosti dominantnej alely Rb génu sa u dieťaťa (heterozygota) nádorová predispozícia zdedená po jednom z rodičov najprv neprejavuje. Ak však u takéhoto dieťaťa dôjde k náhodnej mutácií a funkčnej eliminácii aj druhej alely Rb génu, v bunkách sietnice dieťaťa sa začne tvoriť nádor. Tento proces sa odborne nazýva strata heterozygotnosti a označuje sa skratkou LOH (z angl. loss of heterozygozity).
Aký je rozdiel medzi protoonkogénmi a onkogénmi?
Protoonkogény predstavujú skupinu génov, ktoré môžu mutovať, a tak prechádzať z recesívneho stavu do dominantného, pričom spôsobujú zmenu normálnych buniek na bunky nádorové. Mutované verzie protoonkogénov sa nazývajú onkogény a podmieňujú rôzne typy nádorov. Za normálnych okolností protoonkogény kódujú proteíny regulujúce bunkové delenie, bunkovú diferenciáciu a apoptózu (bunkovú samovraždu). Všetky tieto procesy sú veľmi dôležité na zachovanie normálneho vývoja buniek. Protoonkogény sa môžu meniť na onkogénny aj po ich aktivácii vírusmi. Prvý vírus indukujúci nádory objavil v roku 1910 Peyton Rous. Tento vírus vyvoláva u kurčiat špecifický typ nádoru – sarkóm, a preto dostal pomenovanie vírus Rousovho sarkómu. Výsledkom zmeny/aktivácie protoonkogénu na onkogén je nekontrolovateľná proliferácia buniek, znížená bunková diferenciácia a inhibícia apoptózy. V súčasnosti je známych približne 40 ľudských protoonkogénov. Protoonkogény môžu kódovať veľmi širokú paletu proteínov, ktoré majú v bunke rôzne funkcie (napr. signálne molekuly, rastové faktory, povrchové receptory, regulačné gény, atď.). K najznámejším protoonkogénom patrí RAS. Medzi kódované produkty RAS protoonkogénov patria RAS proteíny, ktoré sa nachádzajú v plazmatickej membráne. Onkogén možno teda definovať ako gén, ktorý sa podieľa na regulácii procesov aktivujúcich alebo urýchľujúcich bunkový cyklus (delenie buniek).
Čo spôsobujú mutátorové gény?
Názov mutátorové gény pochádza z anglického názvu „mutator“, čo znamená, že takýto gén veľmi často podlieha genetickej zmene – mutácii. Nezmutované mutátorové gény sú pre každú bunku veľmi dôležité, pretože zabezpečujú správne fungovanie reparačných (opravných) mechanizmov. A sú to práve reparačné mechanizmy, ktorými disponujú naše bunky a ktoré dokážu rozpoznať a odstrániť genetické poškodenie. Mutácie alebo inaktivácie mutátorových génov spôsobujú hromadenie všetkých mutácií v bunke a tak podmieňujú tzv. nestabilitu genómu (jednu z dôležitých podmienok iniciácie karcinogenézy). Zvýšený počet a hromadenie mutácií v bunke je teda jednou z príčin jej malígnej transformácie. Paradoxne mutované mutátorové gény, na rozdiel od onkogénov a mutovaných tumor-supresorových génov, nemusia samotné vždy spôsobiť nekontrolované delenie buniek. Mutácie mutátorových génov môžu však stimulovať zvýšenie (100 – 1 000-násobné) mutability protonkogénov a tumor-supresorových génov. V iných prípadoch ich mutácie vyvolávajú rakovinu. Napríklad medzi mutátorové gény patria tiež gény, ktorých produkty zaisťujú reparáciu DNA vystrihnutím poškodeného úseku DNA (tzv. excíziu). Ich (recesívne) mutácie spôsobujú ochorenie pomenované xeroderma pigmentosum. Ku klinickým prejavom tohto ochorenia patrí zvýšená citlivosť na UV žiarenie, ktorá sa u dieťaťa s touto mutáciou začína objavovať už od 6 mesiacov do 3 rokov. Po pôsobení slnečných lúčov sa na pokožke začínajú objavovať rozsiahle začervenané miesta, ktoré zostávajú po vyhojení tmavo pigmentované. Neskôr sa pokožka stáva suchou, zvráskavenou a sú na nej prítomné mnohé kožné útvary (napr. angiómy, t. j. nezhubné nádory ciev). Koža sa postupne ošupuje a v poslednom štádiu sa na nej objavujú malígne (zhubné) kožné nádory. U niektorých pacientov sa môžu súčasne vyskytovať aj neurologické poruchy. Xeroderma pigmentosum sa dá diagnostikovať aj prenatálne (v tehotenstve) pomocou odberu choriových klkov (výbežky tvoriace súčasť vyvíjajúcej sa placenty) a plodovej vody. Ochorenie je nevyliečiteľné. Dôležitá je hlavne ochrana pred slnečným žiarením.
Epigenetické zmeny
Epigenetické zmeny sú zmeny génovej expresie, ku ktorým dochádza bez zmeny primárnej genetickej informácie. Epigenetické zmeny (napr. metylácia DNA, zmena štruktúry chromatínu, modifikácie histónových proteínov) menia fungovanie génov. Spôsobujú inaktiváciu tumor-supresorových génov alebo zvýšenú expresiu (nadexpresiu) onkogénov. Niektoré gény dokážu kompletne zapnúť alebo vypnúť, alebo ich činnosť len oslabujú. V roku 2006 výskumníci z Univerzity J. Hopkinsa v USA zistili pri pokusoch na myšiach, že nesprávne zapínanie génu IGF2 vyvolávalo vznik karcinómu hrubého čreva. (Tento gén kóduje proteín, ktorý hrá dôležitú úlohu počas rastu a vývoja človeka a reguluje rast a delenie buniek rôznych tkanív. Je predovšetkým aktívny počas vnútromaternicového vývoja a menej po narodení dieťaťa).
Záverom treba ešte raz zdôrazniť, že základným mechanizmom tumorigenézy/karcinogenézy je nahromadenie (akumulácia) genetických a epigenetických zmien. Karcinogenéza teda predstavuje dlhodobý viacúrovňový proces v priebehu ktorého sa v bunkách kumulujú genetické a epigenetické zmeny, čo v konečnom dôsledku spôsobuje genetickú nestabilitu. Výsledkom týchto genetických a epigenetických zmien je narušenie rovnováhy medzi bunkovou proliferáciou, apoptózou, diferenciáciou, starnutím a mechanizmami kontrolujúcimi tieto bunkové procesy, čím dochádza k postupnej neoplastickej (nádorovej) transformácii buniek.
Autor: prof. RNDr. Eva Miadoková, DrSc. pre redakciu Veda na dosah, Katedra genetiky Prírodovedeckej fakulty Univerzity Komenského v Bratislave
Ilustračné foto: Pixabay.com
Foto v článku: Wikipedia
Redigovala a uverejnila: VČ









